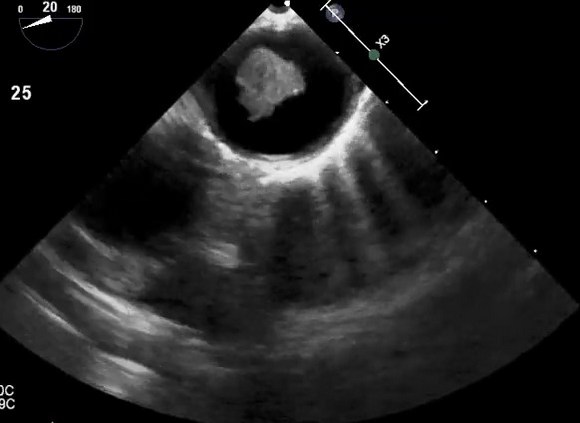
Атерома грудного отдела аорты обычно адекватно не визуализируется с помощью трансторакальной эхокардиографии и чаще всего в заключении пишут об уплотнении аорты. Таким образом, предпочтительным методом визуализации является ЧПЭхоКГ. Обычно аорта делится на три части: восходящая часть, дуга аорты и нисходящая аорта. С точки зрения риска церебральной эмболии наибольший интерес представляют восходящая грудная аорта и дуга аорты, проксимальнее места начала левой общей сонной артерии. При чреспищеводной эхокардиографии корень аорты лучше всего виден в продольной оси аортального клапана (
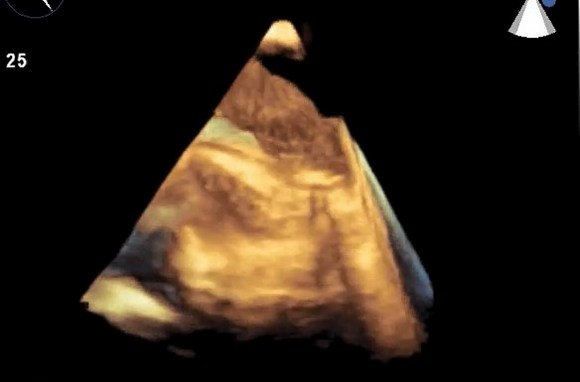
120°). Незначительное выдвижение датчика с уменьшением угла поворота (
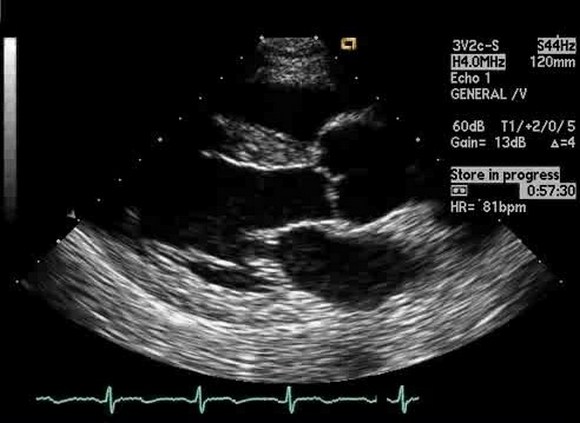
90–100°) даст удовлетворительную визуализацию по длинной оси восходящей аорты в виде трубчатой структуры. На стыке верхней восходящей аорты и дуги аорты имеется эхокардиографическое слепое пятно из-за взаимного расположения левого главного бронха. Визуализация нисходящей аорты начинается в трансжелудочном разрезе.
- Эхокардиографическое обследование при уплотнении аорты
- Ассоциация атеромы грудной аорты и инсульта на эхокардиографии
- Эмболия во время манипуляции с аортой
- Ведение пациентов с атеромой аорты
- Общий подход к оценке атеросклероза аорты на эхокардиографии
- Влияние эхокардиографии на ведение пациентов
- Кардиоэмболические события, связанные с вмешательством
- Новая пероральная антикоагулянтная терапия (NOAC)
- 📸 Видео
Эхокардиографическое обследование при уплотнении аорты
Видео:Возрастной стеноз аортального клапанаСкачать

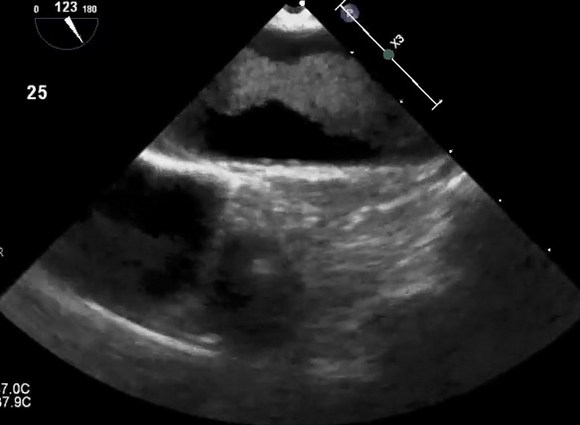
Атеросклеротические изменения грудной аорты все чаще признаются потенциально важным источником эмболии. Обычно сообщается о вращении ультразвукового зонда, при котором нисходящая грудная аорта попадает в окно визуализации. Нисходящая аорта находится позади и очень близко к верхней части желудка и пищевода, и глубина плоскости изображения должна быть отрегулирована для увеличения аорты.
Зонд постепенно извлекается, чтобы визуализировать всю нисходящую аорту грудного отдела, которая при 0° вращения появляется на ее короткой оси. Любое отклонение от нормы, начиная с уплотнения стенок, следует оценивать по его короткой и длинной осям с визуализацией при вращении 0 ° и 90 ° соответственно. Когда зонд введен на глубину примерно на 20 см от резцов, начнет появляться дуга аорты. Лучше всего это визуализировать, повернув зонд кпереди, чтобы открыть вид по длинной оси аорты и визуализировать истоки магистральных сосудов. Визуализация дуги аорты обычно сохраняется до конца исследования, поскольку многие пациенты испытывают рефлекторное рвотное движение от датчика в этом положении и считается его наиболее неудобной частью исследования, требующей его удаления. Эхокардиография может отличить слой интима-медиа сосуда от окружающих тканей, а также обнаруживает изменение между прилегающими тканями и яркой адвентицией. Поэтому для целей количественной оценки стандартно измерять толщину до уровня ярких адвентиций и маркировать это как толщину «атеромы» при уплотнении аорты. Традиционно атерома аорты классифицируется с использованием балльной системы I–IV, хотя, вероятно, лучше измерить глубину (толщину) бляшки и описать ее характеристики (наличие участков изъязвления, кальциноза, сидячей или педункулированной (на ножке) и / или степени поражения, подвижность атеромы). При гистологическом сравнении чреспищеводная эхокардиография при уплотнении аорты показала хорошую корреляцию в разделении нормального и минимального утолщения интимы от более сложных атером (93% совпадение) со 100% совпадением в обнаружении мобильного тромба.
Ассоциация атеромы грудной аорты и инсульта на эхокардиографии
Наблюдательные серии случай-контроль показали значительно более высокую распространенность сложной атеромы (подвижная или изъязвленная бляшка и бляшка толщиной> 4 мм) у пациентов с инсультом (21–27%) по сравнению с контрольной группой (4–13%). В проспективных исследованиях частота инсульта через 1 год у пациентов с выступающей атеромой составила 12%, а частота всех эмболических событий — 33%. Комбинация фибрилляции предсердий и сложной аортальной бляшки связана с более высоким риском инсульта (12–20% в течение 1 года) по сравнению с риском инсульта 1–2% для пациентов с фибрилляцией предсердий без значительного уплотнения аорты и бляшек. Независимо от антикоагуляции или аспирина, это еще одно свидетельство того, что независимый значительный эмболический потенциал связан с атеромой аорты. На распространенность инсульта или других эмболических событий, по-видимому, влияет морфология бляшек. Размер бляшек (толщина), кальцификация атеромы и их подвижность — все это важные характеристики. Увеличение толщины атеромы на эхокардиографии связано с более высоким риском инсульта с порогом 4 мм, в частности, связано со значительно более высоким риском инсульта. Значение видимого изъязвления бляшек неясно с имеющимися данными, предполагающими, что изъязвление в более тонких бляшках связано с повышенным риском, в то время как эта взаимосвязь не значима в более толстых (> 4 мм) бляшках. Наличие кальцификации в бляшках связано со снижением риска эмболических событий, что, вероятно, объясняется тем фактом, что кальцификация, скорее всего, представляет собой наличие более хронических фиброзных бляшек с меньшим содержанием липидов. Мобильные компоненты атеромы аорты также связаны с повышенным риском эмболии с эхопатологической корреляцией, предполагающей, что эти мобильные элементы являются тромбом. Основываясь на текущих данных, похоже, что большинство эмболических событий, связанных с атеросклерозом аорты, являются вторичными по отношению к эмболизации тромбом, который образовался на этих атеросклеротических поражениях.
Читайте также: Замена шлангов отопителя ваз 2110 16 клапанов
Эмболия во время манипуляции с аортой
Существует риск эмболии при манипуляциях на аорте во время кардиохирургических операций или катетеризации левых отделов сердца. Эмболические осложнения при катетеризации сердца редки (частота инсульта 0,5%). Однако, когда все же возникают эмболические осложнения, часто встречается атерома аорты. Сообщаемая частота эмболических осложнений во время кардиохирургических вмешательств с использованием искусственного кровообращения составляет 2–7%. Пациенты с атеромой аорты> 5 мм на ЧПЭхоКГ имеют значительно более высокий риск интраоперационного инсульта. Интраоперационная или эпикардиальная эхокардиография используется для оценки аорты, чтобы помочь стратифицировать риск этих пациентов и найти безопасную точку для введения канюли и пережатия.
При эпикардиальной эхокардиографии используется высокочастотный малогабаритный (трансторакальный) датчик, покрытый стерильной оболочкой, помещенный непосредственно на аорту для визуализации восходящей аорты и дуги аорты с отличным разрешением. «Стойка» (перчатка, заполненная физиологическим раствором) может увеличить расстояние между датчиком и аортой, обеспечивая удовлетворительную визуализацию передней стенки, которую бывает трудно увидеть (слишком близко), если датчик размещен непосредственно на аорте.
Ведение пациентов с атеромой аорты
Видео:Болезни аортального клапана: аортальный стеноз, недостаточность аортального клапана.Скачать

Не существует единого мнения относительно оптимального ведения пациентов со сложной атеромой аорты. Использование антитромботических агентов и / или антикоагулянтов представляется логичным, учитывая ключевую роль тромба в эмболических событиях. Терапия аспирином обычно назначается всем пациентам со значительным атеросклеротическим заболеванием. Также обычно рассматриваются ингибиторы HMGCo-A-редуктазы (статины) с их документально подтвержденными преимуществами у людей с атеросклерозом. Уменьшение частоты инсульта было зарегистрировано у пациентов с гиперлипидемией, а также у пациентов с более «нормальным» уровнем холестерина. Несмотря на то, что антикоагулянтная терапия не была проспективно оценена для пациентов с атеромой аорты, данные наблюдений предполагают, что она, вероятно, полезна.
Тромбэктомия и эндартерэктомия сложной атеромы дуги аорты могут рассматриваться как хорошие кандидаты на хирургическое вмешательство с рецидивирующими эмболическими событиями, несмотря на оптимальную медикаментозную терапию. Однако такой подход связан с высоким уровнем неврологических и сосудистых осложнений.
Общий подход к оценке атеросклероза аорты на эхокардиографии
Сердечно-сосудистый источник эмболии все чаще выявляется при обследовании пациентов с острой церебральной, периферической или висцеральной ишемией. Большинство отчетов сосредоточено на источниках эмболии у пациентов с инсультом. Как уже отмечалось, уровень доказательств, демонстрирующих убедительные причины и следствия, ограничен, и эти потенциальные источники лучше всего описывать как «ассоциации», а не как убедительные причины. Важно тщательно оценить пациентов на предмет всех потенциальных источников, и не исключено обнаружение у него более одного потенциального источника, тем более что распространенность многих из этих факторов увеличивается с возрастом. Кроме того, как заболевание сонной артерии, так и атерома грудной аорты являются проявлениями одного и того же патологического процесса, и неудивительно, что пациенты со значительным атеросклерозом сонных артерий имеют более высокую распространенность атеросклероза дуги аорты, чем пациенты без заболевания сонных артерий. Следовательно, может потребоваться оценка аорты, особенно если неврологическое событие контралатерально стенозу сонной артерии или если заболевание сонной артерии связано с периферическими или висцеральными эмболами.
Читайте также: Запчасти клапана для митсубиси
Влияние эхокардиографии на ведение пациентов
Как только наступила острая фаза неврологического события, основная цель — выявить любые потенциально излечимые источники и предотвратить повторяющиеся, потенциально фатальные события. Данные показывают, что частота рецидивов для всех подтипов инсульта составляет 9,4% в год и 10% для криптогенного инсульта. Сообщается, что чреспищеводная эхокардиография полезна для стратификации риска у пациентов после инсульта. Одна серия пациентов, за которыми наблюдали в течение 2 лет и которые были разделены на группы низкого и высокого риска (на основании наличия хотя бы одного вероятного или возможного фактора риска эмболии при ЧПЭхоКГ), показала, что пациенты из группы низкого риска чувствовали себя значительно лучше (выживаемость составила 92% против 63%, p = 0,04). В исследовании STEPS (242 пациента после ЧПЭхоКГ по поводу необъяснимого инсульта)при уплотнении аорты, демонстрировала атерому аорты и дилатацию ЛЖ, выявила подгруппы с высоким риском повторного инсульта при лечении одним аспирином, что указывает на потенциальную роль эхокардиографии в помощи в выборе терапии и ее влиянии на исход после индексного церебрального события. Однако необходимы проспективные исследования, чтобы определить, можно ли преобразовать идентификацию предикторов рецидива инсульта в улучшение результатов лечения пациентов.
Кардиоэмболические события, связанные с вмешательством
При расширенном использовании вмешательств во время лечении сердечно-сосудистых заболеваний наблюдались побочные эффекты, такие как ятрогенные инсульты и системная эмболизация. Коронарная ангиография, одна из наиболее широко используемых процедур, наряду с чрескожной реваскуляризацией, произвела революцию в лечении ИБС. Однако, когда инсульт усложняет эти процедуры, он сводит на нет получаемые от него преимущества и ускоряет нанесение вреда. Использование определенных методов может помочь снизить этот риск. Исследователи показали, что промывание катетеров в нисходящей аорте с последующим продвижением к корню аорты значительно снизило частоту микроэмболизации по сравнению со стандартным препарированием катетера в восходящей аорте.
Кроме того, сведение к минимуму количества маневров с катетером значительно снижает риск микроэмболизации головного мозга. Также, было обнаружено, что левый лучевой доступ имеет меньший риск эмболизации мозга, чем правый лучевой. Этот результат был в основном связан с меньшим количеством маневров катетера, необходимых для левостороннего лучевого доступа. Более того, технологические достижения позволили ввести новые процедуры в мир лечения сердечно-сосудистых заболеваний. Одной из таких сложных процедур является чрескожное транскатетерное введение аортального клапана (TAVI), которое стало предпочтительной процедурой для пациентов с аортальным стенозом высокого хирургического риска. Было показано, что TAVI связан с повышенным риском сосудистых эмболий (частота 30-дневного инсульта колеблется от 2 до 5%). Точно так же аблация фибрилляции предсердий в настоящее время выполняется все чаще. Многие обсервационные исследования показали, что тихие инсульты вторичны по отношению к этим процедурам.
Следовательно, взвешивая риск сосудистых событий, связанных с этими вмешательствами, ожидается, что с развитием технологий, повышением квалификации и тщательным отбором пациентов эти процедуры должны стать более безопасными со временем. Примером модификации технологии для уменьшения инсульта является введение кругового катетера MER при абляции фибрилляции предсердий.
Новая пероральная антикоагулянтная терапия (NOAC)
Недавнее внедрение новых методов лечения пероральными антикоагулянтами (NOAC) предоставило больше возможностей для пациентов с неклапанной фибрилляцией предсердий. Основные преимущества NOAC заключаются в том, что эти агенты не требуют мониторинга, имеют быстрое начало действия и значительно снижают риск внутричерепного кровотечения по сравнению с пероральным антагонистом витамина K (VKA). Основные недостатки этих агентов заключаются в том, что их использование противопоказано при тяжелой почечной недостаточности и отсутствии антидота, чтобы обратить их действие, когда это необходимо. В дополнение к использованию NOAC в качестве хронической замены VKA, недавно исследование XVeRT показало, что пероральный ривароксабан можно безопасно использовать в качестве возможной альтернативы терапии VKA для предотвращения тромбоэмболических событий у пациентов, подвергающихся плановой кардиоверсии.
Предпринята попытка расширить использование NOAC для механических сердечных клапанов. Испытание дабигатрана по сравнению с варфарином у пациентов с механическими клапанами сердца было преждевременно прекращено после включения 252 пациентов из-за повышенного количества случаев тромбоэмболии и кровотечений среди пациентов в группе дабигатрана. Аналогичным образом, исследование RE-ALIGN было прекращено на раннем этапе из-за более высоких тромботических осложнений у пациентов с механическими сердечными клапанами, получавших дабигатран, по сравнению с пациентами, получавшими варфарин. Таким образом, до сих пор данные не подтверждают использование терапии NOAC у пациентов с механическими сердечными клапанами.
📸 Видео
Эхокардиография. Фиброз аортального клапанаСкачать

Из-за чего происходит уплотнение аорты🧐?Скачать

Эхокардиография. Створки аортального клапанаСкачать

УПЛОТНЕНИЕ АОРТЫСкачать

Недостаточность аортального клапана.Скачать

Протезирование аортального клапанаСкачать

Эхокардиография. Кальциноз аортального клапана. Аортальный стеноз 3 степени. Диффузный гипокинезСкачать

Вопросы врачу. Аортальная недостаточностьСкачать

Кальциноз сосудов - хороший признак?Скачать

Пролапс митрального клапана. Что это и как быть.Скачать

Разбираем показатели вашего ЭХОКГ.Скачать

Кальциноз фиброзного кольца митрального клапанаСкачать

КАЛЬЦИНОЗ СЕРДЦА , СОСУДОВ , АОРТЫ как лечить .Скачать

УЗИ сердца. Двустворчатый аортальный клапанСкачать

Борис Тодуров: чем опасны пороки клапанов сердца и как их распознать? ► О пороках сердца #5Скачать

Порок сердца. Стеноз аортального клапана.Скачать

Что такое фиброз?Скачать

Смертельное заболевание по УЗИ сердца #ShortsСкачать