- Атрезия трикуспидального клапана у плода выживет ли ребенок
- Атрезия трикуспидального клапана у детей
- Ведение детей с атрезией трикуспидального клапана
- Атрезия трикуспидального клапана у плода выживет ли ребенок
- Видео ЭхоКГ при атрезии трикуспидального клапана у плода
- Атрезия трехстворчатого клапана. Принцип операции Фонтена
- Атрезия трехстворчатого клапана
- Что же может быть сделано и — когда?
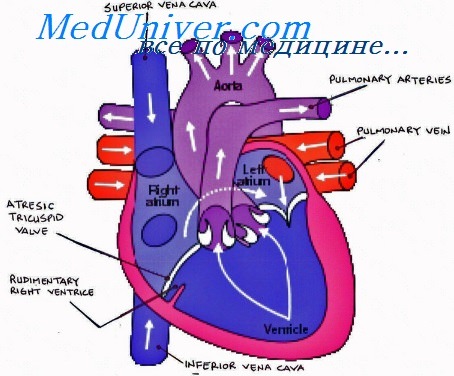
Атрезия трикуспидального клапана у плода выживет ли ребенок
Наиболее часто отмечается среди детей с синдромом Дауна. При полном ДПЖП определяется дефект в середине сердца с единичным пятистворчатым клапаном между предсердием и желудочками, который располагается вдоль всего предсердно-желудочкового соединения и имеет склонность к пропусканию крови обратно. В связи с тем что имеется крупный дефект, развивается лёгочная гипертензия.
Признаки полного ДПЖП:
• Проявление в антенатальном периоде на скри-нинговом УЗИ.
• Цианоз при рождении или сердечная недостаточность на 2-3-й нед жизни.
• Отсутствие признаков, не выслушиваются шумы, повреждение выявляется при рутинном скринин-говом ЭхоКГ новорождённых детей с синдромом Дауна. Всегда имеется подъём сегмента ST выше изолинии на ЭКГ.
Ведение пациентов заключается в лекарственной коррекции сердечной недостаточности (как и при крупном ДМЖП) и хирургическом восстановлении в возрасте 3-6 мес.
Атрезия трикуспидального клапана у детей
При атрезии трикуспидального клапана эффективно работает только левый желудочек, при этом правый желудочек маленький и не функционирующий.
Клинические признаки атрезии трикуспидального клапана у детей. При этой патологии в левом предсердии обычно смешиваются артериальная кровь системного кровотока и возвратная венозная кровь из лёгочного кровотока. Проявляется цианозом у новорождённых в период, зависимый от состояния протока, или у детей, вполне благополучных при рождении, у которых потом развивается цианоз или останавливается дыхание.
Ведение детей с атрезией трикуспидального клапана
Раннее паллиативное лечение проводится для поддержания адекватного притока крови к лёгким при низком давлении.
• Шунт Блелока-Тауссига (между подключичной и лёгочной артериями) — у детей с тяжёлым цианозом.
• Перевязывание лёгочной артерии — для уменьшения лёгочного кровотока, если имеется нарушение дыхания.
Проведение полной хирургической коррекции невозможно, поскольку имеется лишь один эффективно функционирующий желудочек. Проводится паллиативное лечение (операция Гленна или Геми-Фонтана, в процессе которых выполняется соединение верхней полой вены с лёгочной артерией после 6-месячного возраста, и операция Фонтана, также направленная на соединение верхней полой вены с лёгочной артерией в возрасте 3-5 лет).
Таким образом, левый желудочек проводит кровь по всему телу, и системное венозное давление осуществляет обеспечение притока крови к лёгким.
Операция Фонтана приводит к недостаточно идеальному функциональному исходу, однако преимущество заключается в уменьшении цианоза и удалении долгосрочной нагрузки объёмом на единственный функционирующий желудочек.
У большинства детей наступает быстрое выздоровление после проведённого хирургического лечения, и они возвращаются в детские сады или школы в течение месяца. Практически всем потребуется антибиотикопрофилактика для предотвращения бактериального эндокардита.
Устойчивость к физической нагрузке будет различной, и большинству детей можно предоставить возможность определить их собственные лимиты. Ограничение физической нагрузки рекомендуется только для детей с тяжёлым резидуальным аортальным стенозом и при дисфункции желудочков.
Большинство детей наблюдаются в дальнейшем в специализированных кардиологических клиниках. Большинство из них ведут нормальную жизнь без ограничений, однако любые изменения симптомов, например снижение толерантности к физической нагрузке или сильное сердцебиение, требуют дальнейших исследований.
Возрастает число подростков и молодых людей, которым требуется проведение ревизии хирургического вмешательства, произведённого в раннем детстве. Наиболее распространёнными причинами для этого являются смена искусственных клапанов и освобождение стеноза от постхирургической линии швов, к примеру повторная коарктация или стеноз лёгочной артерии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Атрезия трикуспидального клапана у плода выживет ли ребенок
а) Терминология:
• Отсутствие отверстия ТК:
о ПП не сообщается с ПЖ
б) Лучевая диагностика атрезии трикуспидального клапана:
• На четырехкамерном срезе ПЖ уменьшен, а ТК имеет форму тарелки
• В результате аномалии обязательно возникает сброс крови из ПП в ЛП
• Как правило, присутствует ДМЖП:
о Попадание крови из ЛЖ в малый круг кровообращения возможно только при условии правильного взаимоотношения магистральных сосудов
• Сопутствующие пороки развития сердца обнаруживают с частотой до 20%:
о Характерны стеноз или атрезия легочной артерии
Читайте также: Клапан выпускной daewoo matiz
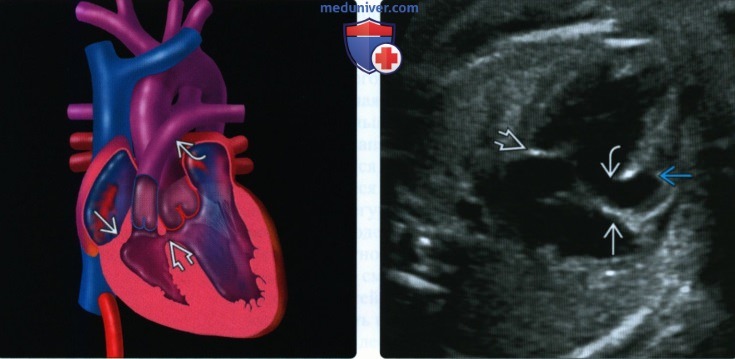
(Справа) УЗИ. Характерная картина атрезии ТК. Митральный клапан не изменен. Кровь поступает в гипоплазированный ПЖ через ДМЖП. 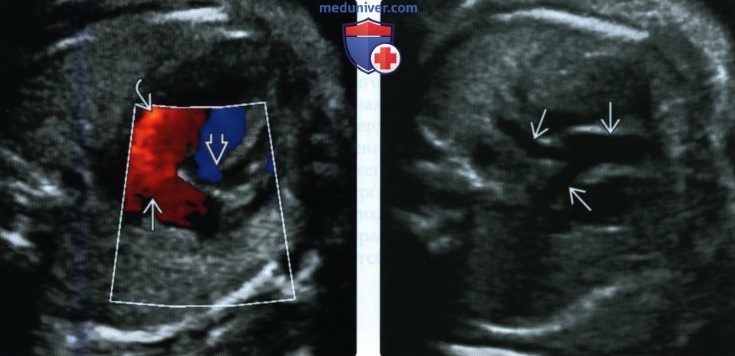
(Справа) УЗИ выносящих трактов. Визуализируются главная легочная артерия и ее ветви, отходящие от ПЖ. Снимок является подтверждением правильного взаимоотношения и отсутствия транспозиции магистральных сосудов, что важно установить до рождения ребенка.
в) Патологоанатомические особенности:
• Тип I: взаимоотношение магистральных артерий не нарушено (72%)
• Тип II: D-транспозиция (25%)
• Тип III: L-транспозиция (3%)
• Тип IV: общий артериальный ствол (редко)
г) Клинические особенности:
• При отсутствии лечения смертность в течение 1-го года жизни составляет 90%
• Показатели выживаемости среди пациентов с атрезией ТК, диагностированной пренатально, с учетом современных достижений хирургии:
о Выживаемость к 1 мес. жизни — 91%, к 1 году — 83%
о К 10 годам — 83%
• Неблагоприятные прогностические факторы:
о Наличие хромосомной аномалии или синдрома
о Использование экстракорпоральной мембранной оксигенации
д) Особенности диагностики:
• Если визуализируются ТК в форме тарелки и гипоплазия ПЖ:
о Оценивают вентрикулоартериальные соединения
о Оценивают наличие и размеры ДМЖП, обструкции выносящего тракта
о В случае D-транспозиции обнаруживают обструкцию аорты
Видео ЭхоКГ при атрезии трикуспидального клапана у плода
Редактор: Искандер Милевски. Дата обновления публикации: 9.10.2021
Атрезия трехстворчатого клапана. Принцип операции Фонтена
Слово означает полное отсутствие нормального сообщения между сердечными камерами или между ними и отходящими от них магистральными сосудами, а иногда — и отсутствие отделов самих сосудов. Термин атрезия применяется к трехстворчатому, митральному, аортальному и легочному клапанным отверстиям, к аорте и легочной артерии.
Другой термин — — означает, что сообщение есть, но оно уменьшено в размерах в сравнении с нормальным. Говорят о гипоплазии трехстворчатого или митрального клапанов, отделов аорты, легочной артерии, но так же и о размерах полости одного из желудочков ().
Атрезия трехстворчатого клапана
В нормально развитом сердце соединяет правое предсердие с правым желудочком. При атрезии этот клапан не развился и на его месте имеется плотная мембрана, через которую поток крови пройти никак не может. Поскольку этот участок закрыт, то у плода не развился и тоже отсутствует весь приточный отдел правого желудочка, т.е. первый из двух конусов, образующих желудочек. Таким образом, измененным оказывается не только клапан, но и весь правый желудочек — у него отсутствует половина.
Однако, и плод, и родившийся ребенок могут с этим жить, во всяком случае, какое-то время. Шунтирование крови и ее смешивание в сердце происходит через дефекты в перегородках.
Из полых вен кровь попадает в нормальное правое предсердие. Но вход в желудочек — закрыт. Остается один путь: сквозь дефект межпредсердной перегородки — в левое предсердие. Затем через нормально развитый митральный клапан кровь поступает в левый желудочек. А вот здесь открыто два пути. Один — в аорту, другой — через дефект межжелудочковой перегородки — в оставшуюся часть правого желудочка (второй из конусов, который нормально развит) и отсюда — в легочную артерию и легкие.
Потоки крови в левом желудочке смешиваются — венозная кровь из полых вен, достигшая желудочка таким сложным путем, смешивается с артериальной кровью, пришедшей из вен легких.
Путь дальнейшего ее «распределения» зависит от того, куда легче идти основному потоку: в аорту или через дефект межжелудочковой перегородки — в легочную артерию и легкие. Кровь так и разделяется на два рукава, и разница в объеме двух потоков зависит от разницы сопротивления сосудов тела (т.е. большого круга кровообращения) и сопротивления, создаваемого дефектом перегородки.
Читайте также: Регулировка клапанов двигателя змз 405
В большинстве случаев существенно больший объем крови проходит в аорту и меньший — в легкие. Во-первых, значительная часть крови остается недонасыщенной, и у ребенка будет цианоз. Степень этого цианоза, однако, не столь выражена, как при полной транспозиции магистральных сосудов — ведь в желудочке все-таки происходит смешение артериальной и венозной крови. А, во-вторых, левый желудочек работает на оба круга, т.к. правого почти нет. Нагрузка, которая выпала на его долю — тяжелая, и очень она может быстро вызвать недостаточность кровообращения в большом круге — одышку, увеличение печени, отеки и т.д.
В сущности, и качество, и продолжительность жизни таких детей зависит от величины кровотока в легких, т.е. определяется размером дефектов в межжелудочковой и межпредсердной перегородках — этих, в данном случае, естественных шунтов «во спасение».
Со временем, по мере роста ребенка (и сердца) положение ухудшается, т.к. в легкие идет все меньше крови. Нарастает цианоз и около 90% детей не доживут до своего первого дня рождения, если им не оказать хирургическую помощь.
Оставшиеся 10% имеют достаточно большой дефект в перегородке, и кровоток в легкие у них нормальный, а иногда даже и усиленный. Они чувствуют себя неплохо, относительно нормально развиваются и почти не синюшные. Такие дети могут прожить более 10-15 лет, но у них постепенно будут развиваться признаки сердечной недостаточности и нарастать цианоз со всеми его осложнениями и последствиями.
Что же может быть сделано и — когда?
В лечении атрезии трехстворчатого клапана хирургия, особенно за последние два десятилетия, добилась значительных успехов и тактика лечения, выбор операции и времени ее проведения сегодня разработаны достаточно, чтобы добиться убедительных хороших результатов. Но нужно понимать, что, если у сердца изначально не было одного из четырех клапанов и большого участка одного из желудочков, то их сделать заново нельзя. Таких методов пока нет.
Поэтому весь процесс лечения сведется к созданию иных, более оптимальных путей для кровотока. Другими словами, лечение будет облегчающим, «паллиативным», и его нельзя выполнить в один раз, а надо постепенно готовить и сердце, и легкие к новым, более нормальным условиям кровотока, чем те, в которых они оказались при рождении.
Детям с выраженным цианозом в течение первых месяцев надо сделать операцию наложения анастомоза между большим и малым кругами кровообращения, как это описано для тетрады Фалло. Эта операция значительно улучшит их состояние на первых порах. Они начнут развиваться, будут выглядеть и вести себя соответственно возрасту, пройдет синюшность.
Но это — только первый, «жизнеспасающий» этап. Если больше ничего не делать, ребенок скоро снова станет очень больным и, чем хуже будет его состояние, тем более рискованными будут последующие этапы лечения.
Между первым и вторым годом жизни становится возможным выполнение второго этапа, а именно, снятие первого анастомоза и создание другого пути для венозной крови в легкие — прямое соединение верхней полой вены с легочной артерией, в обход правой половины сердца. Почему этого не делают сразу? Дело в том, что в первые месяцы жизни сопротивление сосудистого русла легких может оказаться слишком высоким. Подумайте, ведь давление в венах очень низкое — 5-7 мм ртутного столба, а мы хотим, чтобы оно было достаточным, чтобы без сердечного «насоса» кровь пассивно текла в легочную артерию. Для этого между венами и сосудами легких должна быть разница в сопротивлении и давлении, иначе кровь в легкие просто не потечет.
Бывают ситуации, и их довольно много, когда мы выполняем эту операцию — двунаправленный кавапульмональный анастомоз на первом году жизни, без ранее выполненного системно-легочного анастомоза. Данное клиническое решение принимает Ваш кардиолог и кардиохирург, вырабатывая таким образом наилучшую тактику лечения Вашего ребенка.
Мы останавливаемся на этом столь подробно, т.к. сам принцип так называемого применяется сегодня широко и при других пороках, когда сердце изменено настолько, что порок невозможно исправить хирургически. Так вот на этом, втором этапе, верхняя полая вена соединяется с легочной артерией таким образом, что кровь из нее поступает в оба легких. Иными словами, кровь от верхней половины тела уже идет туда, куда надо. Но пока — только от половины.
Читайте также: Когда зажаты клапана что происходит
Дети обычно хорошо переносят операцию. Эта операция не только улучшит состояние ребенка, но и подготовит сердце и сосуды легких к третьей, заключительной стадии в процессе лечения — соединения нижней полой вены с легочной артерией.
Наилучшим моментом для выполнения третьей операции будет возраст 4-5 лет, хотя иногда ее делают и раньше этого срока.
Эта операция делается с искусственным кровообращением и заключается во вшивании большой заплаты или протеза в нижнюю полую вену одним концом и в легочную артерию — другим. Таким образом, теперь вся венозная кровь от всего организма идет в легкие, а окисленная в полном объеме — в левые отделы сердца, т.е. в его теперь единственный желудочек.
Эту операцию называют операцией Фонтена — по имени французского хирурга, который ее предложил.
Сегодня ее применяют не только при , но и при многих сложных врожденных пороках, когда хирургическое создание двух равноценных желудочков невозможно. Эта операция произвела революцию в лечении пороков, которые совсем недавно считались неоперабельными . Больным с такими пороками просто отказывали даже в самых лучших кардиоцентрах. Сегодня все изменилось, и благодаря операции Фонтена можно помочь и уже помогли тысячам больных. Сам принцип такого подхода — принцип Фонтена — однако, всего лишь паллиация, пусть и хорошо функционирующая. Операция Фонтена, т.е. заключительный этап хирургического лечения нельзя назвать «радикальной коррекцией» (как, например, при закрытии дефекта межпредсердной перегородки), к ней больше подходит название «постоянной паллиации», т.е. это не исправление порока, а последняя возможность максимальной в данном случае нормализации кровообращения. Человек живет без правого желудочка, а кровь пассивно течет в легкие из венозной системы. Здоров ли этот человек? Может ли он переносить те физические и психологические нагрузки, которые ожидают его в жизни? О том, что сегодня известно об этом, мы поговорим немного ниже, а сейчас вернемся к .
Как ни парадоксально это выглядит, но, чем тяжелее состояние ребенка с этим пороком изначально, тем яснее путь его лечения. Но каждый ребенок — индивидуален, и можно столкнуться с различными вариантами и сочетаниями внутрисердечных нарушений: слишком маленьким дефектом между предсердиями, слишком большим межжелудочковым сообщением, врожденным сужением легочной артерии и ее ветвей и т.д.
В каждом случае надо выбрать наиболее рациональный и безопасный способ помощи. Иногда следует вначале расширить межпредсердный дефект в рентгенохирургическом кабинете, иногда — наложить манжетку на легочный ствол, чтобы уменьшить легочный кровоток и предупредить развитие других осложнений. Сегодня все эти методы хорошо известны, но тактика лечения и последовательность — индивидуальны. Главное, чтобы ребенок сразу попал в специализированное учреждение, где есть соответствующий опыт.
Сможет ли ребенок долго и нормально жить, не имея одной из частей сердца — правого желудочка? Оказывается, сможет, и долго, и совсем неплохо. Сегодняшняя статистика говорит о том, что подавляющее большинство больных, живущих с «фонтеновским кровообращением», относятся к так называемому функциональному классу I-II степени, т.е. практически здоровы. Примерно четверти из них, оперированных 10 и более лет назад, потребовались повторные операции по замене ранее вшитых протезов, но сегодня по мере совершенствования техники операции, можно надеяться, что число таких случаев значительно уменьшится.
Главным осложнением в отдаленные сроки после операции является так называемая , выражающаяся в отеках, скоплении жидкости в полостях, потере белка. Оно поддается консервативному лечению. Так что будем оптимистами.
Понятно, что ребенок должен постоянно (минимум раз в полгода) наблюдаться у детского кардиолога, даже если нет видимых осложнений. Ребенок – не инвалид ни в коем случае, но наблюдать его должен квалифицированный и опытный врач.
В любом случае, вашему ребенку со сложнейшим ВПС было сделано все, что может предложить современная медицина, и это — такая же победа врачей, как и ваша.