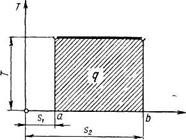
Выберите 2 бесконечно, слегка наведите точки А и 6 и опустите к оси «вертикаль ai n bc». Бес- Конечно, небольшая платформа aby такая же, как Ty3, но、 Таз = ОД. Если мы интегрируем это уравнение по всему пути процесса от /до 2、 Поэтому диаграмму T-s иногда называют тепловой диаграммой, поскольку она представляет тепло, которое подается в процесс в областях, ограниченных диаграммой T-S, кривой процесса, абсциссой и полярным полем.
И СС проявляет те же признаки, а увеличение энтропии указывает на то, что тепло подается к рабочему телу извне во время процесса(процесс происходит с точки 2).Уменьшение энтропии, напротив, характеризует процесс с отводом тепла от рабочего тела в окружающую среду (движение процесса из точки 2 в точку 1). На рис. 7.2 точка рисуется, касательной ае кривой процесса. Угол a, касательный к оси абсцисс, принадлежит прямоугольному треугольнику aOe. Нога ai определяет температуру рабочей жидкости в процессе времени a.
- Кроме того, для политропного процесса можно описать нижнюю часть зависимости. Если выравнять справа эти зависимости и определить теплоемкость политропного процесса, то: Или если (7.13) дано、 Но судя по фигуре. 7.2, но он может видеть это (8 ″ = Е 1 Представляет собой касательную кривую процесса в точке A. Эта касательная определяет истинную теплоемкость процесса при температуре T. положительные значения (да, положительная теплоемкость соответствует отрицательным значениям, отрицательные значения (рис.7.2, б). Цикл диаграммы Т-5 представлен замкнутой кривой. На рисунке 7.3 показан цикл a-b-c-y-a.
Для каких значений времени будет справедливо полученное уравнение? Людмила Фирмаль
Если направление процесса в цикле находится в направлении движения по часовой стрелке, то есть по пути a-b-c-s-a, pl. abce [а]、 Внешне подключается к рабочей жидкости, а огве — / е Жара в течение дня ПЛ ж! ce (a. рисунок 7.2. Таким образом, тепловой эквивалент работы, выполняемой рабочим телом в цикле, представлен площадью/ C = — dg = квадрат. Absé Читайте также: Датчик коленчатого вала чери фора
































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Видео:Работа с ТS диаграммой хладогентаСкачать

ЭНТРОПИЯ ГАЗОВ. TS -ДИАГРАММА
Для более полного исследования термодинамических процессов и облегчения исследований и расчетов в термодинамику был введен математически немецким физиком Р. Клаузиусом еще один параметр состояния газа (шестой) — энтропия S. Его название происходит от греческого слова превращение.
Энтропию измеряют в тех же единицах, что и массовую теплоемкость, т. е. в кДж/кг . град
(или при использовании внесистемной единицы ккал/кг . град). Энтропию обозначают буквой s для 1 кг газа и буквой S для G кг.
Рис.5 Изотермический процесс в TS-диаграмме
Таким образом, в термодинамике используются три основных параметра — р, vи Т (давление,удельный объем и температура) и три дополнительных — и, i и s (внутренняя энергия, энтальпия и энтропия).
С точки зрения графического изображения энтропия как параметр состояния газа может быть использована в прямоугольной системе координат Ts, где в соответствующем масштабе s — энтропию — откладывают по оси абсцисс, а Т — абсолютную температуру — по оси ординат. Такая диаграмма в координатах Tsназывается Тs-диаграммой Т = const, линия процесса 1—2 (рис.6 ) будет проходить параллельно оси s. В таком случае площадь прямоугольника в некотором масштабе будет измерять количество тепла q, участвующего в изометрическом процессе, т. е. q = (s2 –s1)T, где s1 — энтропия 1 кг газа в начальном состоянии; s2 — энтропия 1 кг газа в конечном состоянии;
Отсюда следует, что s2 –s1 = или
Рис.6 Количество тепла в TS-диаграмме
Таким образом, для графического изображения количества тепла в Ts-диаграмме пользуются двумя параметрами — энтропией и абсолютной температурой, при этом количество сообщенного или отнятого тепла, получаемого при произвольных изменениях состояния, выражается площадями диаграммы Ts подобно тому, как работа выражается площадями в PV-диаграмме. Отношение Δq/T – (приведенная теплота) является качественной характеристикой процессов преобразования тепла.
Для изменения параметров идеального газа в равновесных процессах:
Следовательно, под энтропией тела можно понимать величину, изменение которой Δs в любом элементарном термодинамическом процессе равно отношению внешнего тепла Δq, участвующего в этом процессе, к абсолютной температуре тела T.
Читайте также: Валы для рейсмуса метабо
Энтропия является мерой потери работоспособности системы вследствие необратимости реальных процессов. Потеря работы от необратимого процесса прямо пропорциональна возрастанию энтропии.
Изменение энтропии, как и изменение внутренней энергии, энтальпии и некоторых других термодинамических величин не зависит от пути протекания процесса, а зависит лишь от начального и конечного состояний рабочего тела.
В уравнении абсолютная температура Т — величина всегда положительная. Следовательно, Δq и Δs имеют одинаковые знаки, т. е. если Δq положительно, то и Δs положительно и, наоборот, если Δq отрицательно, то и Δs отрицательно. Таким образом, в обратимых процессах с подводом тепла (Δq >0) энтропия газа увеличивается, а в обратимых процессах с отводом тепла (Δq
Получим формулы, позволяющие вычислять изменение энтропии идеального газа. Для этого проинтегрируем уравнение [41],
Например, для изохорного процесса при cυ = const, S2-S1 = cυ ln +R ln
Из уравнения Клапейрона, записанного для состояний 1 и 2, следует:
. После подстановки отношений Т2/Т1 и υ2/υ1 в полученное выражение получим следующие формулы для изменения энтропии идеального газа:
Для адиабатного процесса, протекающего без теплообмена газа с внешней средой,
так как в этом процессе q = 0, то Δs = 0. Следовательно, адиабатный процесс в Ts-диаграмме изображается прямой вертикальной линией, перпендикулярной оси s. Для политропного процесса
где с — теплоемкость политропного процесса.
| рис. 7 Политропные процессы в TS -диаграмме |
С позиций кинетической теории газов энтропию можно определить как меру неупорядоченности системы. Когда от системы при постоянном давлении отводится теплота, энтропия уменьшается, а упорядоченность в системе повышается. Это можно наглядно продемонстрировать на примере превращения газообразного вещества в твердое.
Молекулы газа движутся беспорядочно. Когда газ при отводе теплоты и соответствующем уменьшении энтропии конденсируется в жидкость, молекулы занимают более определенное положение (некоторое время молекула жидкости колеблется около какого-то положения равновесия, затем положение равновесия смещается и т. д., т. е. происходят одновременно медленные перемещения молекул и их колебания внутри малых объемов). При дальнейшем понижении температуры жидкости энтропия уменьшается, а тепловое движение молекул становится все менее интенсивным. Наконец, жидкость затвердевает, что связано с дальнейшим уменьшением энтропии, неупорядоченность становится еще меньше (молекулы только колеблются около средних равновесных положений.
Дата добавления: 2014-12-24 ; просмотров: 18539 ;
Видео:Лекция 3 Построение цикла кондиционера на диаграммеСкачать
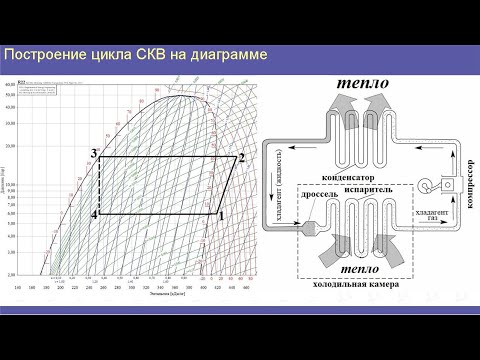
Рабочий процесс парокомпрессионной холодильной установки в координатах Т-s
Рис. 2.5. Схема диаграммы Т-s
Читайте также: Подшипник вторичного вала кпп тойота королла 150
В процессе R –с пары агента адиабатно сжимаются до рс в первой ступени компрессора и вытесняются в промежуточный водяной или воздушный охладитель, где остывают от Тс до Тd при рс = const. Во второй ступени пары сжимаются также адиабатно в процессе d-е до давления в конденсаторе рк и Те. Перегретый пар точки e охлаждается в конденсаторе при рК = const до состояния сухого насыщенного пара в точке 2, а затем конденсируется и полностью превращается в жидкость (х = 0) в точке 3 при ТК. Жидкий аммиак затем поступает в водяной охладитель, а фреон в регенеративный охладитель, где охлаждаются от ТЗ = ТК до Т4 при рК = const. Затем жидкий агент поступает в регулирующий вентиль, где дросселируется при h = const в процессе 4-5 от рК, Т4 до р0, Т0. В охлаждающей батарее (или испарителе) агент кипит при р0, Т0 в процессе 5-1 и превращается в сухой насыщенный пар точки 1.
Охлаждение жидкого агента перед дросселированием повышает холодопроизводительность установки. Так без охлаждения жидкого агента дросселирование протекало бы процессом 3-4′. При этом после дросселирования х4′ = 0,27. Это значит, что 0,27 кг жидкого агента испарилось за счет своей теплоты, а 1 – х4′ = 0,73 кг в охлаждающей батарее. При охлаждении в точке 5 х = 0,2. Это значит, что самоиспарилось при дросселировании только 0,2 кг агента, а в охлаждающей батарее испарилось уже 0,8 кг, что больше чем без охлаждения на 0,07 кг. По диаграмме Т-s можно найти все параметры необходимые для расчета холодильной установки или теплового насоса. Однако при решении задач в контрольной работе следует применять диаграмму l g p-h. Схема диаграммы l g p-h приведена на рис. 2.6. По оси ординат отложены абсолютные давления р, в МПа, а по оси абцисс значения энтальпии h в кДж/кг. Изобарные процессы проходят в планшетке координат горизонтально, процессы дросселирования h = const – вертикально. Изотермы в области жидкости представляются вертикальными. На рабочей диаграмме это не показывается. В области влажного насыщенного пара, между линиями х = 0 и х = 1, изотермы совпадают с изобарами, а в области перегретого пара они круто опускаются вниз штрих пунктирными линиями. Из точки К опущены линии постоянной степени сухости от х =0,1 до х = 0,9. В области перегретого пара нанесены адиабаты (изоэнтропы s = const). Они начинаются от линии х = 1 и направлены вверх вправо в виде сплошных линий.
- Свежие записи
- Чем отличается двухтактный мотор от четырехтактного
- Сколько масла заливать в редуктор мотоблока
- Какие моторы бывают у стиральных машин
- Какие валы отсутствуют в двухвальной кпп
- Как снять стопорную шайбу с вала
- Правообладателям
- Политика конфиденциальности
📺 Видео
Работа с диаграммой воды и водяного параСкачать
Диаграмма с двумя осями для отображения "разношерстных" показателейСкачать
Сводные диаграммыСкачать
Центробежный компрессорСкачать
Как работает кондиционер схема автокондиционера. car air conditioning. aire acondicionado automotrizСкачать
Точность NanoVNA F Зачем нужна диаграмма СмитаСкачать
Принцип работы системы умягчения водыСкачать
09 Фазовые диаграммы двухкомп сист 1 принципы и мех смесьСкачать
Как создать диаграмму в Excel?Скачать
🧾Mathcad + RefProp #5. Построение T-s диаграммыСкачать
Только не говори никому.. Как легко можно восстановить жидкокристаллический экран..Скачать
Диаграмма Смита (Smith chart) – это очень просто!Скачать
Вагнеровцы после обороны Бахмута #shortsСкачать
6, Диаграммы статической и динамической остойчивостиСкачать
Мощность и Индикаторная диаграмма двухтактного двигателя. Индицирование и оценка работы ДВС.Скачать
Штормовая диаграмма | Инструкция к программеСкачать
Точечная диаграммаСкачать
13. ОСНОВЫ ТЕПЛОТЕХНИКИ. Влажный воздух. Точка росы. Гигрометр. I-d Диаграмма Рамзина. Решение задачСкачать