б) Лучевая диагностика:
• Локализация ТК не изменена
• Створки клапана утолщены, узловатые или имеют неправильную форму:
о В результате возникает недостаточность ТК → дилатация ПП и повышение риска водянки плода
• Часто сопровождается стенозом или атрезией легочной артерии
• Оценивают ритмичность сердечных сокращений
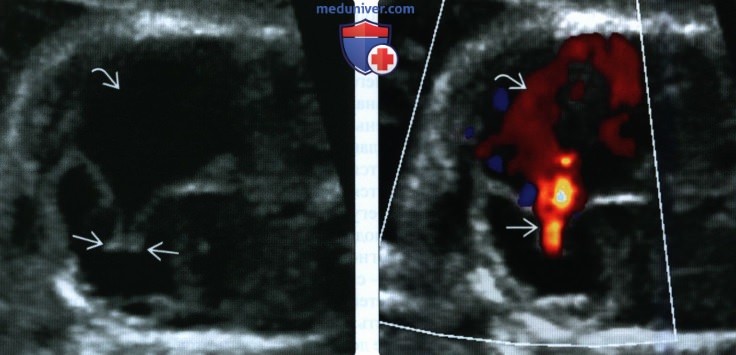
(Справа) Тот же случай. ЦДК в той же плоскости. Определяется выраженная трикуспидальная регургитация. ПП значительно расширено, в полости визуализируются турбулентные потоки. 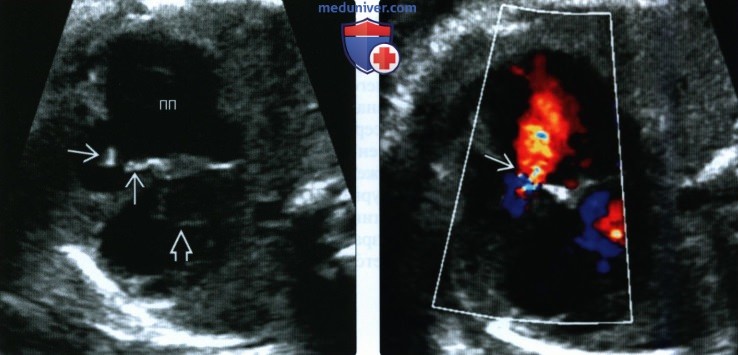
(Справа) Тот же случай. ЦДК. Определяется выраженная трикуспидальная регургитация, вызванная неполным смыканием створок. Выраженная регургитация, приводящая к увеличению ПП и развитию водянки плода, связана с неблагоприятным прогнозом.
в) Дифференциальная диагностика:
• Аномалия Эбштейна:
о Также сопровождается дисплазией и недостаточностью ТК, но отличительная особенность — смещение септальной и задней створок по направлению к верхушке сердца
о Происходит «атриализация» ПЖ
о Уменьшение функциональной части ПЖ
г) Патологоанатомические особенности:
• Патофизиология аномалии Эбштейна и дисплазии ТК схожа
д) Клинические особенности:
• Может впервые проявиться цианозом у новорожденного вследствие сброса крови слева направо на уровне предсердий:
о Громкий систолический регургитирующий шум при аускультации
• Возможно самопроизвольное снижение тяжести нарушений:
о Причина — стремительное снижение легочного сосудистого сопротивления после рождения
• Выраженная регургитация, диагностированная внутриутробно или у новорожденного, связана с неблагоприятным прогнозом:
о Чаще всего — смерть плода
о Исход у детей, родившихся живыми, неблагоприятный -выживаемость более 1 мес. составляет 20%
• Пациентам с сердечной недостаточностью и выраженным цианозом без улучшения со временем и после снижения легочного сосудистого сопротивления требуется хирургическое лечение
- Видео ЭхоКГ при дисплазии трикуспидального клапана у плода
- Дисплазия трехстворчатого клапана у новорожденных
- Клиническая симптоматика трикуспидальной недостаточности.
- Диагностика недостаточности трехстворчатого клапана.
- Лечение трикуспидальной недостаточности.
- Дисплазия трехстворчатого клапана у новорожденных
- ПРЕНАТАЛЬНАЯ ДИАГНОСТИКА ПОРОКОВ СЕРДЦА, ТЕЧЕНИЕ БЕРЕМЕННОСТИ, КЛИНИЧЕСКИЕ СЛУЧАИ СОЧЕТАНИЯ КАРДИАЛЬНОЙ ПАТОЛОГИИ ПЛОДА С АНОМАЛИЯМИ ДРУГИХ ОРГАНОВ
Видео ЭхоКГ при дисплазии трикуспидального клапана у плода
Редактор: Искандер Милевски. Дата обновления публикации: 9.10.2021
Дисплазия трехстворчатого клапана у новорожденных
В основе недостаточности трикуспидального клапана у новорожденных могут лежать разнообразные причины. К ним относятся органические изменения структур клапана (аномалия Эбштейна, дисплазия клапана), повышенное давление в правом желудочке (клапанный или инфундибулярный легочный стеноз, персистирующая легочная гипертензия, объемные перегрузки правых отделов сердца вследствие артериовенозного шунта или значительной анемии), выраженная гипоксия миокарда. В последнее время выделяют синдром транзиторной трикуспидальной недостаточности, который диагностируют при отсутствии другой врожденной патологии сердца.
При фетальной эхокардиографии трикуспидальную регургитацию обнаруживают у 6-7% плодов, однако лишь в 20% этих случаев она является значительной (занимает всю систолу, максимальная скорость потока более 2 м/с) и в большинстве наблюдений быстро исчезает после родов. В постнатальном периоде изолированная трикуспидальная регургитация при отсутствии анатомических изменений внутрисердечных структур, как правило, сопровождает дисфункцию правого желудочка вследствие перенесенной перинатальной гипоксии; частота трикуспидальной регургитации среди таких новорожденных составляет около 7%. Морфологическим субстратом патологии может быть дискинезия желудочка, особенно папиллярных мышц; примерно у 15% больных находят инфаркт папиллярной мышцы, чаще передней. В некоторых случаях это приводит к ее разрыву или отрыву хорды.
Нарушения гемодинамики связаны с возникающей объемной перегрузкой правого предсердия и правого желудочка, сопровождающейся застойной сердечной недостаточностью. Массивная трикуспидальная регургитация приводит к снижению антеградного выброса из желудочка, вплоть до развития функциональной легочной атрезии. Нарядусэтим возникает сброс венозной крови через овальное окно в левые отделы сердца, что приводит к артериальной гипоксемии.
Читайте также: Ошибка 0172 ваз 2115 8 клапанов причина
Естественное течение патологии обычно благоприятное, в большинстве случаев трикуспидальная регургитация уменьшается и исчезает в течение нескольких недель, по мере физиологического снижения давления в легочной артерии и улучшения условий работы правого желудочка. Однако при наличии инфаркта папиллярной мышцы, особенно сопровождающегося отрывом хорд, возможен летальный исход в первые 7 дней жизни.
Клиническая симптоматика трикуспидальной недостаточности.
Заболевание напоминает персистирующую легочную гипертензию. Как правило, у данных новорожденных имеются указания на неблагоприятное течение беременности, перенесенную гипоксию. В первые часы после рождения определяются цианоз (без существенной реакции на повышение концентрации кислорода во вдыхаемой смеси) и систолический шум над областью сердца; быстро развивается сердечная недостаточность. Шум может отсутствовать при выраженной депрессии правого желудочка. При анализе р02 и S02 выявляется артериальная гипоксемия.
Диагностика недостаточности трехстворчатого клапана.
Электрокардиография. Наряду с типичной для новорожденных правограммой определяется диффузная ишемия миокарда, преимущественно в субэндокардиальной зоне, отражающая последствия перинатальной гипоксии.
Рентгенография грудной клетки. Легочный кровоток обеднен. Сердце увеличено за счет правых отделов, преимущественно правого предсердия.
Эхокардиография. Характерной является дилатация правого предсердия и правого желудочка. В некоторых случаях расширен и левый желудочек. Межпредсердная перегородка выбухает в сторону левого предсердия; через овальное окно регистрируется сброс крови справа налево. На трикуспидальном клапане имеется регургитация, величина которой нередко достигает значительной степени (рис. 3-4 на цветной вкладке). Суммарная фракция выброса правого желудочка может быть существенно не изменена, однако ударный выброс в легочную артерию и давление в ней значительно снижены.
При исследовании остальных структур сердца врожденных пороков их развития не выявляют. В некоторых случаях определяется функционирующий ОАП.
Лечение трикуспидальной недостаточности.
Базовая терапия включает снижение физической активности больного, поддержание нормальной температуры тела, оксигенотерапию. Показано назначение инотропных препаратов (допамин 4—6 мкг/кг/мин, адреналин 0,1 —0,2 мкг/кг/мин), иногда — мочегонных препаратов. Это сочетают с применением препаратов-вазодилататоров легочного русла (простагландины, гидралазин).
В тяжелых случаях проводят искусственную вентиляцию легких с гипервентиляцией, повышенной концентрацией кислорода, низким давлением на вдохе и в конце выдоха, введением оксида азота.
В случаях отрыва хорд выполняют хирургическое вмешательство с целью их восстановления.
— Вернуться в оглавление раздела «Кардиология.»
Дисплазия трехстворчатого клапана у новорожденных
ПРЕНАТАЛЬНАЯ ДИАГНОСТИКА ПОРОКОВ СЕРДЦА, ТЕЧЕНИЕ БЕРЕМЕННОСТИ, КЛИНИЧЕСКИЕ СЛУЧАИ СОЧЕТАНИЯ КАРДИАЛЬНОЙ ПАТОЛОГИИ ПЛОДА С АНОМАЛИЯМИ ДРУГИХ ОРГАНОВ
Сердечная патология является одной из основных причин детской смертности и находится на втором месте среди причин младенческой смертности. Частота составляет 8 случаев на 1000 новорожденных [1, 2].
Неблагоприятный прогноз для жизни представляют сложные врожденные пороки сердца (ВПС). Под термином «сложный» понимают такие сердечные аномалии, как гипоплазированные камеры сердца, атрезии клапанов, аномальное отхождение магистральных сосудов, единственный желудочек, то есть изменения в сердце, при которых невозможно выполнить полную хирургическую коррекцию [3].
Критические пороки сердца, требующие хирургического вмешательства в ранний неонатальный период, составляют 25 % от всех врожденных сердечных аномалий. В первую неделю умирает 29 % новорожденных, к концу первого года жизни – 87 % [4].
Первое ультразвуковое скрининговое обследование (11–13 недель) является важным осмотром. В случае обнаружения увеличения толщины воротникового пространства, отклонения сердечной оси, рекомендуется расширенное обследование сердца (фетальная эхокардиография). При рутинном ультразвуковом исследовании лишь в 40 % выявляются пороки сердца у плодов, при том что детальный осмотр позволяет выявлять до 90 % сердечных пороков внутриутробно. Для своевременного выявления врожденных пороков сердца необходимо детально обследовать сердце плода ультразвуковым методом при втором скрининговом обследовании (18–22 недели) [5, 6].
Применяя фетальную эхокардиографию, возможно определить структуру порока и спрогнозировать исход для плода [7]. Особенно это касается сложных пороков сердца, так как имеет место позднее выявление патологии, при осмотре неонатологом в родильном доме или после выписки домой [8].
Читайте также: Каково состояние полулунных клапанов в третьей фазе сердечного цикла
Данная тема является актуальной. Врачи пренатальной диагностики встречаются с трудностями точного определения структуры сердечных пороков, что связано с большой вариабельностью кардиальной аномалии у плодов.
Задачей врачей-гинекологов является правильная тактика ведения беременной после установки диагноза, так как своевременная хирургическая помощь спасает жизни детей и влияет на качество дальнейшей жизни.
Цель исследования: проанализировать течение беременности при выявлении кардиальной патологии у плодов, определить точность внутриутробной диагностики, описать случаи сочетания сердечных пороков с патологией развития других органов плода.
Материалы и методы исследования
В центре диагностики матери и плода «Family» г. Бишкек с января 2019 г. по ноябрь 2020 г. было осмотрено 48 беременных женщин с пороками сердца плода, требующими хирургической коррекции после рождения. Всем новорожденным было проведено эхокардиографическое обследование после родов врачами-кардиологами для уточнения структуры пороков. В случаях прерывания беременности, для подтверждения диагноза проводилось патологоанатомическое вскрытие.
Осмотр беременных выполнялся на ультразвуковых аппаратах General Electric (GE) Voluson E8 и E10, c использованием программы fetal heart. Также использовалась программа STIC (постобработка снимков, полученных в режиме объемного сканирования), основным являлся двумерный режим с цветовым и импульсным доплеровским картированием. У всех пациентов было получено информированное согласие на участие в нашем исследовании. Результаты были обработаны путем вычисления относительных величин (в %).
Результаты исследования и их обсуждение
Среди 48 плодов с ВПС сложные пороки сердца были в 40 случаях (83,3 %). Из общего количества умерли после родов 23 ребенка (47,9 %). Прервали беременность 3 женщины (6,2 %), в двух случаях проводилось патологоанатомическое вскрытие плодов. Третья беременная после заключения медицинской комиссии прервала беременность в сроке 31 неделя, в связи с плохим прогнозом для жизни ребенка. Диагноз был подтвержден методом эхокардиографии.
Из факторов риска, по анализам обменных карт, острые респираторные вирусные инфекции (ОРВИ) до 12 недели перенесли 14 женщин (29,1 %), ОРВИ во втором триместре перенесли 4 женщины (8,3 %). Анемия легкой степени имела место в 12 случаях (25,0 %), хроническая ревматическая болезнь сердца у матери – один случай (2,0 %). Многоплодные беременности как фактор риска в нашем случае встречались в двух случаях (4,1 %), обе дихориальные, диамниотические двойни.
Количество плодов мужского пола составило – 31 (64,5 %), женского 17 (35,4 %). Маловесными (вес менее 2600 г.) родились 9 детей (18,7 %), из них 8 имели сочетание порока сердца с ненормальным развитием других органов, в одном случае порок сердца был изолированным.
При ультразвуковом исследовании фетоплацентарное нарушение кровотока 1 степени выявлено у одной беременной (2,0 %), задержка внутриутробного развития у 4 (8,3 %), маловодие у 2 (4,1 %), многоводие у 5 (10,4 %), причем избыточное количество вод во всех случаях сочеталось с множественными пороками развития.
Сложности при ультразвуковом осмотре вызывали неправильное положение плода, большой срок гестации (после 35 недель), многоводие, маловодие. Необходимо отметить, что технология STIC информативна при осмотрах четырехкамерной проекции сердца (пороки атривентрикулярных клапанов, гипоплазии желудочков, дефекты межжелудочковой перегородки). Для осмотра выходных трактов желудочков, особенно при повороте оси сердца, осмотр в двумерном режиме является предпочтительным. Также для осмотра органов других систем маловодие и неудобное положение плода являются помехами для трехмерного ультразвука.
Структура выявленных пороков оказалась многообразна. Нами были диагностированы: у 5 плодов (10,4 %) двойное отхождение сосудов от правого желудочка, аномалия Эбштейна – 1 (2,0 %), транспозиция магистральных сосудов – 3 (6,2 %), стеноз легочной артерии – 7 (14,5 %), изолированный перимембранозный дефект межжелудочковой перегородки – 3 (6,2 %), декстрапозиция аорты с дефектом межжелудочковой перегородки – 5 (10,4 %), атрезия легочной артерии – 4 (8,3 %), атриовентрикулярный канал –5 (10,4 %), тетрада Фалло – 6 (12,5 %), перерыв дуги аорты – 1 (2,0 %), атрезия трикуспидального клапана – 1 (2,0 %), атрезия митрального клапана – 4 (8,3 %), из них в двух случаях аортальный клапан был атрезирован, также в двух случаях имелось двойное отхождение сосудов от правого желудочка. Коарктация аорты составила один случай (2,0 %), единственный желудочек – 2 (4,1 %).
Читайте также: Клапан запорный dn40 msv s
После рождения вскрытие проводилось в одном случае – ребенку с аномалией Эбштейна, который умер в родильном доме на вторые сутки. Согласно заключению патологоанатома, причиной смерти стала острая сердечная недостаточность, дилатация полостей сердца, острый венозный застой внутренних органов.
В двух случаях единственного желудочка диагностика оказалась затруднительной как внутриутробно, так и после родов. В первом случае трикуспидальный клапан был атрезирован и полость правого желудочка практически отсутствовала, также имелся единый сосуд, исходящий из функционально единого желудочка. После родов рекомендовалась компьютерная томография для уточнения диагноза. При телефонном разговоре с матерью мы узнали, что в возрасте 10 месяцев ребенок еще не прошел полного обследования, но в развитии значительно отставал, не мог переворачиваться и самостоятельно не сидел.
Во втором случае мы диагностировали правосформированное, праворасположенное сердце в сочетании с единым атриовентрикулярным клапаном, двойным отхождением сосудов от правого желудочка, ребенок умер в первый месяц жизни.
Среди плодов с кардиальной патологией в 6 случаях (12,5 %) было сочетание с хромосомными аберрациями и генетическим заболеванием: синдромом Дауна – 4 случая, синдромом Ди Джорджи – один случай; также наблюдался один случай редкой генетической патологии (синдром Холта – Орама, наследственное заболевание, сочетание порока сердца с отсутствием первого пальца на кистях обеих рук до аплазии лучевой кости).
После родов успешно прооперированы были двое детей с тетрадой Фалло, также двое детей со стенозом клапана легочной артерии. Один ребенок с диагнозом двойного отхождения сосудов от правого желудочка благополучно оперирован в Турции. К сожалению, в случаях транспозиции магистральных сосудов и единственного желудочка детям было отказано в проведении оперативного лечения как местными, так и зарубежными хирургами в связи с высоким риском смерти сразу после операции.
Приводим наблюдение о несовпадении нашего диагноза с эхокардиографическим заключением после родов. В нашем центре при плановом обследовании на 30 неделе беременности был установлен диагноз коарктации аорты с дефектом межжелудочковой перегородки. В родильном доме при проведении эхокардиографии был выявлен только дефект мышечной перегородки, коарктация была исключена. Ребенок умер через 2 недели после родов, от вскрытия родители отказались. Мы пришли к выводу, что портативные ультразвуковые аппараты, на которых обследуют детей в родильных домах, могут вызывать сложности визуализации и неполную диагностику, что связано с менее четким изображением, чем на стационарном оборудовании.
По данным литературы, внутриутробная диагностика пороков сердца возможна с 13 недели беременности, в частности таких сложных для выявления ВПС, как атрезия легочной артерии [9]. В нашем центре плод с атрезией легочной артерии и дефектом межжелудочковой перегородки был выявлен в 18 недель беременности. Данная беременность была прервана в связи с неблагоприятным прогнозом для жизни. Патологоанатомическое вскрытие подтвердило диагноз. По нашему мнению, 18 неделя беременности (второе скрининговое обследование) является наиболее ранним сроком для точного определения структуры порока. Связано это с тем, что магистральные сосуды сердца плода плохо видны в сроки первого скринингового обследования, что может приводить к неточной диагностике.
Из 48 случаев с ВПС 16 плодов (33,3 %) имели множественные пороки развития, причем такие изменения, как гидроцефалия, укорочение трубчатых костей, выявлялись на сроках после 30 недель. А случаи атрезии ануса были обнаружены только при рождении детей. Таким образом, выявление любых изменений в сердце является поводом для обязательного повторного ультразвукового обследования в сроки 25–30 недель (таблица).
Сочетание врожденных пороков сердца с аномалиями других органов
Сочетание ВПС с патологией других органов
Сроки выявления ВПС (неделя беременности), исход
1. Перимембранозный дефект межжелудочковой перегородки




