Ожидаемая продолжительность жизни детей с врожденными пороками сердца благодаря современной оперативной хирургии, высокому уровню интенсивной терапии, широкому применению неинвазивных методов диагностики значительно увеличилась, и сегодня многие дети с такими пороками доживают до взрослого состояния. Поэтому необходимо, чтобы терапевты и кардиологи были хорошо знакомы с эхокардиографической картиной важнейших врожденных пороков, как до-, так и послеоперационной. Именно этой задаче посвящена настоящая глава.
а) Симптоматика. Врожденные пороки сердца, как следует из названия, присутствуют у детей уже при рождении. Но это не означает, что после рождения они непременно проявляются клинически. Нередко у ребенка выявляют лишь морфологические изменения, лежащие в основе того или иного порока сердца или крупных сосудов, а проявляются они позднее в связи с развитием вторичных нарушений. У многих больных симптоматика порока отчетливо проявляется лишь во взрослом периоде в связи с прогрессирующим нарушением гемодинамики.
б) Лечение. Коррекция врожденных пороков сердца, как правило, требует выполнения открытого хирургического или рентгенохирургического, или интервенционного, вмешательства. Оптимальные сроки хирургической коррекции обычно соответствуют детскому возрасту. Во многих случаях такая коррекция представляет собой компромисс между возможностью устранения или исправления морфологического субстрата порока и развившимися вторичными изменениями и функциональными нарушениями.
Поэтому в статьях на сайте мы считаем необходимым описать также у лиц молодого возраста послеоперационную картину наиболее частых пороков сердца, коррекция которых была уже выполнена в детстве.
Если из-за стертой клинической картины врожденный порок сердца в детстве остался недиагностированным, то оперативную коррекцию следует выполнить позже, когда устанавливают диагноз или при первых же клинических проявлениях.
Врожденные пороки клапанов сердца и стеноз сосудов могут клинически проявляться уже при рождении. Они обычно сочетаются с другими пороками сердца. В детском возрасте они встречаются реже, чем пороки, проявляющиеся патологическим сбросом крови, но у взрослых частота их растет. Дальнейшее описание этих пороков приводится в разделе «Врожденный стеноз аортального клапана — двустворчатый аортальный клапан».
в) Врожденные пороки полулунных клапанов. Причиной врожденных пороков полулунных клапанов сердца является неполное разделение трех створок полулунных клапанов. Эти пороки представляют собой континуум от неполного разделения комиссуры между створками через двустворчатый клапан вплоть до клапана, состоящего из одной створки, и даже атрезии клапана. Чем более выражен дефект развития клапана, тем раньше появляются симптомы и тем тяжелее клиническая картина. Поэтому понятно, что у взрослых встречаются лишь легкие формы врожденных пороков полулунных клапанов.
г) Врожденный стеноз аортального клапана — двустворчатый аортальный клапан. Врожденный стеноз аортального клапана у взрослых — наиболее частый врожденный порок сердца. У детей этот порок встречается довольно редко. Такое расхождение в частоте можно объяснить тем, что хотя анатомически клапан и состоит из двух створок, функция его длительное время остается компенсированной и поэтому симптомы дисфункции клапана отсутствуют. Часто вначале отмечается легкая недостаточность клапана, а в дальнейшем постепенно развивается стеноз и к 60 годам у 53% больных с данным пороком имеется клиническая картина гемодинамически значимого стеноза.
1. Патологическая анатомия. Наиболее частым пороком аортального клапана и в то же время наиболее частым врожденным пороком сердца является двустворчатый аортальный клапан. Он имеется у 1-2% людей. Нередко двустворчатый аортальный клапан сочетается со стенозом перешейка аорты. При данном пороке имеются лишь две створки неодинакового размера. Часто на одной створке имеется шов или ложная комиссура. Поскольку края створок прямые и не вибрируют, как полулунные створки нормального клапана, то систолическое открытие может быть неполным. Вследствие этого площадь отверстия открытого клапана уменьшена.
Из-за сниженной растяжимости створок пораженного клапана функция его в детском возрасте может оставаться компенсированной и клинические проявления порока отсутствуют. Позднее из-за постепенного фиброза и частичного сращения створок развиваются стеноз и недостаточность аортального клапана.
2. Гемодинамика. Уменьшение площади отверстия аортального клапана приводит к появлению трансаортального градиента давления, что вызывает повышение давления в левом желудочке. Это в свою очередь приводит к гипертрофии левого желудочка, повышению напряжения его стенки и появлению вторичных изменений, например расширения полости и относительной митральной недостаточности.
Особенности движения стенозированного клапана можно видеть также на видеозаписи.
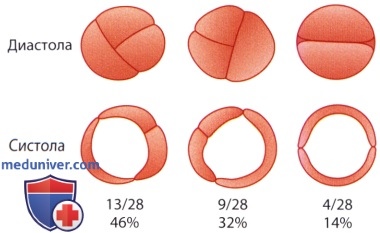
Схематическое изображение различных вариантов двустворчатого аортального клапана по Brandenburg и соавт..
При наиболее частой форме (13/28) имеется шов между правой и левой коронарными створками аортального клапана; реже (9/28) отмечается сращение между нейтральной и правой коронарной створками.
Относительно редко (4/28) встречается истинно двустворчатая форма клапана.
3. Двумерная эхокардиография. Морфологические изменения аортального клапана у взрослых наиболее отчетливо видны при многопроекционной ЧПЭ. Иногда при этом исследовании удается непосредственно измерить площадь клапанного отверстия. Нередко отмечается смещение открытия правой коронарной створки, которая может пролабировать в диастолу в выносящий тракт левого желудочка. На видеозаписи выше видны асимметрия аортального клапана, систолическое выбухание и диастолическое пролабирование в выносящий тракт левого желудочка. Субаортальная область левого желудочка, как правило, широкая, но при выраженном стенозе аортального клапана может оказаться стенозированной из-за развития гипертрофии межжелудочковой перегородки.
В восходящем отделе аорты, особенно при легком и умеренном стенозе аортального клапана, отмечается постстенотическое расширение.
4. Эхокардиография в М-режиме. Эхокардиографию в М-режиме выполняют для выявления гипертрофии левого желудочка. В типичных случаях при стенозе аортального клапана гипертрофия бывает концентрической, но иногда выявляется асимметричная гипертрофия межжелудочковой перегородки. При врожденном стенозе аортального клапана эхокардиографическая картина левого желудочка при исследовании в М-режиме сравнима с картиной при приобретенном аортальном стенозе. Сама область аортального клапана при этом исследовании часто не изменена. Из-за систолического выбухания относительно податливой створки аортального клапана отмечается хорошая сепарация створок у основания. Нередко отмечается асимметрия линии смыкания створок в корне аорты.
5. Цветовая допплерография. При цветовом допплеровском исследовании отмечается престенотическое ускорение кровотока в выносящем тракте левого желудочка. Струя крови через суженное отверстие аортального клапана часто асимметрична и направлена к правой переднебоковой стенке восходящей аорты. Почти всегда появляется также аортальная недостаточность, которая распознается по обратной струе крови из аорты в выносящий тракт левого желудочка в диастолу.
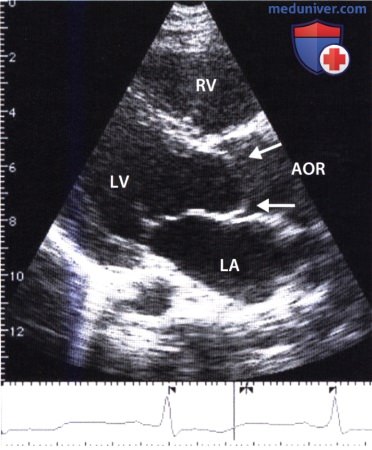
На двумерной эхокардиограмме, зарегистрированной в конце систолы, отчетливо видно неполное открытие аортального клапана в систолу и выбухание его (стрелка).
AOR — корень аорты, LA — левое предсердие, L.V -левый желудочек, LV — правый желудочек. 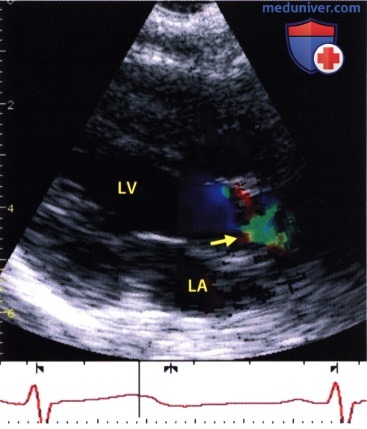
При двумерном цветовом допплеровском сканировании в конце систолы видна струя крови через стенозированный аортальный клапан (стрелка). АО — аорта. 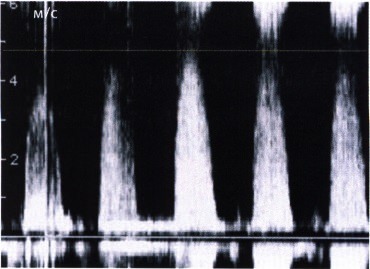
Максимальное значение мгновенного градиента давления, рассчитанное по упрощенному уравнению Бернулли, составило 92 мм рт.ст.
Однако это значение не соответствует градиенту давления, измеренному при катетеризации (Peak-to-Peak), и существенно выше.
6. Спектральная допплерография. Из-за сужения отверстия аортального клапана скорость кровотока через него повышена. Существует нелинейная зависимость между скоростью тока крови и трансаортальным градиентом давления, описываемая уравнением Бернулли. В связи с тем что струя крови через суженный клапан часто бывает направлена к правой переднебоковой стенке восходящей аорты, ее лучше лоцировать, располагая датчик в парастернальной или супрастернальной позиции (при непрерывноволновой допплерографии карандашным датчиком), так как в этой позиции датчика регистрируется максимальная скорость струи.
Читайте также: Генератор ваз 2112 16 клапанов инжектор артикул
Оценка степени стеноза аортального клапана, определяемая по максимальному мгновенному градиенту давления, рассчитанному по упрощенному уравнению Бернулли на основании максимальной скорости трансаортального кровотока, оказывается завышенной по сравнению с оценкой на основании измерения давления при зондировании камер сердца.
7. Другие изменения, выявляемые при ЭхоКГ. Как уже упоминалось, часто при стенозе аортального клапана выявляют также его недостаточность, которая обычно развивается перед появлением клинических симптомов стеноза.
Видео:Вопросы врачу. Двустворчатый аортальный клапанСкачать

Видео ЭхоКГ аортального клапана — оценка, протокол исследования
Редактор: Искандер Милевски. Дата обновления публикации: 29.1.2021
Видео:УЗИ сердца. Двустворчатый аортальный клапанСкачать

Двустворчатый аортальный клапан эхокг заключение
а) Методы исследования и настройка аппарата. В настоящее время используются несколько методов эхокардиографического исследования, с помощью которых можно количественно определить степень аортальной недостаточности. Широко применявшееся до внедрения цветового допплеровского исследования допплерографическое расширенное «картирование» в импульсном режиме для определения степени аортальной недостаточности уже не играет какой-либо роли.
Хроническая аортальная недостаточность приводит к постепенному расширению левого желудочка; это подчеркивает важность определения размера левого желудочка и его сократительной функции для оценки степени аортальной недостаточности. Функция левого желудочка для оценки прогноза играет большую роль, чем степень аортальной регургитации.
С помощью цветовой допплер-ЭхоКГ, которая характеризуется высокой чувствительностью, можно быстро и надежно диагностировать аортальную недостаточность. Для этого сердце обычно исследуют из парастернальной позиции по длинной оси и из апикальной позиции двух- или пятикамерного сердца. По своей чувствительности этот метод превосходит как аускультацию, так и ангиографию. У практически здоровых лиц в 5-10% случаев выявляют небольшую, так называемую «физиологическую» регургитацию, которая занимает лишь раннюю фазу диастолы.
Для более точной оценки степени аортальной недостаточности важную роль играет оптимальная настройка ультразвукового аппарата: цветовое усиление доводят до уровня, при котором достигается максимальная интенсивность цвета струи регургитации без появления артефактов вне струи. Кроме того, рекомендуется по возможности уменьшить угол между ультразвуковым лучом и направлением струи, чтобы получить максимально возможное качество цветового изображения (8-15 МГц). Предел Найквиста сначала устанавливают в диапазоне 0,4-0,7 м/с.
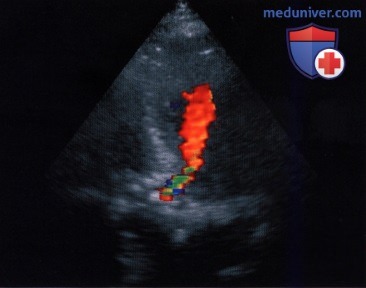
б) Площадь цветового потока. Для количественной оценки аортальной недостаточности широко распространено определение площади струи, лоцируемой методом цветового допплеровского картирования в плоскости двух или пяти камер из апикальной позиции датчика. Однако диагностические возможности данного метода исследования ограничены, поэтому корреляция между длиной, шириной и площадью профильного сечения струи и степенью тяжести аортальной недостаточности слабая. Как известно, площадь профиля струи регургитации зависит от значительно большего числа факторов, например от настройки аппарата, пред- и постнагрузки, типа струи (свободная, «пристеночная»), податливости левого желудочка и аорты. Кроме того, трудно отличить струю аортальной регургитации от входящего диастолического потока из левого предсердия, особенно при сопутствующем митральном стенозе, когда струя аортальной регургитации отклоняется в направлении митрального клапана.
Скрининг. По описанным выше причинам определение площади профильного сечения струи является лишь скрининговым исследованием, которое позволяет дать полуколичественную оценку клапанной недостаточности. Однако предсказательная ценность отрицательного результата исследования высокая, т.е. метод, как правило, позволяет исключить аортальную недостаточность, когда, несмотря на технически корректное «веерообразное» исследование всей плоскости с расположенными в ней клапанами из парастернальной и апикальной позиции датчика, струю регургитации выявить не удается. В то время как небольшая струя, расположенная вблизи аортального клапана, с высокой степенью достоверности позволяет диагностировать легкую аортальную недостаточность, при более интенсивной струе регургитации отличить умеренную аортальную недостаточность от тяжелой обычно бывает невозможно.
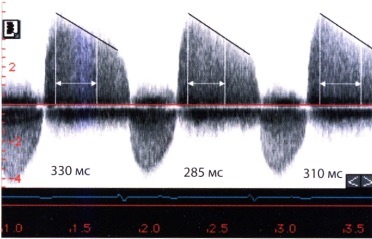
T1/2, в среднем равное 310 мс, у больного с выраженной аортальной недостаточностью.
в) Время полуспада градиента давления (РНТ или T1/2). Для определения времени полуспада градиента давления (РНТ или T1/2) проводят касательную к профилю струи. Известно, что снижение градиента давления зависит от того, как быстро происходит выравнивание давления в аорте и левом желудочке. При тяжелой аортальной недостаточности давление в аорте быстро падает, а в левом желудочке быстро нарастает. Выравнивание давления происходит очень быстро, касательная направлена круто, время полуспада градиента давления короткое. Наоборот, если выравнивание давлений происходит медленно (в случае менее выраженной аортальной недостаточности), время T1/2 становится более продолжительным.
Преимуществом метода является хорошая воспроизводимость результатов. Однако он имеет и недостаток, который состоит в том, что из-за часто отмечающейся эксцентричности струи регургитации ее направление приближается к ортогональному, и поэтому профиль кривой скорости получается недостаточно четким.
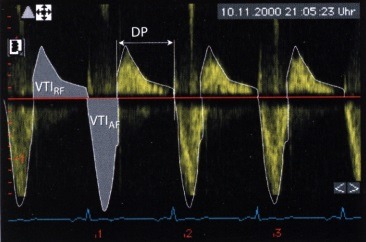
В сравнительном исследовании с помощью допплерографии и катетеризации полостей сердца время T1/2P, как маркер гемодинамически значимой аортальной недостаточности, оказалось Профиль кровотока в нисходящем отделе грудной аорты у больного с выраженной аортальной недостаточностью. Кровоток на протяжении всей диастолы ретроградный, отношение VTIRF/VTIAF=60%. VTIRF — интеграл скорости ретроградного кровотока; VTIAF — интеграл скорости антероградного кровотока.
г) Кровоток в грудной аорте. Еще одним способом количественной оценки аортальной недостаточности является ультразвуковое исследование дуги аорты и ее нисходящего отдела из супрастернальной позиции датчика. В то время как кровь через компетентный аортальный клапан во время диастолы течет в антероградном направлении, при аортальной недостаточности появляется ретроградный ток. По величине обратного диастолического кровотока в аорте можно судить о степени тяжести аортальной недостаточности. С помощью допплерографии в импульсном режиме из супрастернального доступа можно определить кровоток в нисходящей аорте, непосредственно дистальнее места отхождения левой подключичной артерии. Для количественной оценки аортальной недостаточности используют следующие параметры:
— Отношение длительности ретроградного диастолического кровотока к длительности диастолы TRF/TDiast (в процентах).
— Отношение интеграла скорости ретроградного кровотока к интегралу антероградного кровотока VTIRF/VTIAF (в процентах).
Zarauza и соавт. удалось у 45 из 51 больного (90%) получить четкий профиль кровотока в грудной аорте и с его помощью определить указанные выше параметры. В отдельных случаях профиль кровотока можно регистрировать, лоцируя брюшную аорту датчиком, располагаемым под мечевидным отростком. Контрольный объем устанавливают на расстоянии 2-3 см под диафрагмой.
Touche и соавт. и Zarauza и соавт. показали, что почти у всех больных с аортальной недостаточностью высокой степени можно обнаружить голодиастолический ретроградный ток в грудной аорте; отсутствие данного признака, как правило, позволяло исключить гемодинамически значимую аортальную недостаточность. По значению отношения VTIRF/VTIAF. разграничить умеренную аортальную недостаточность от тяжелой можно лишь условно, так как этот параметр зависит не только от степени аортальной регургитации, но и от податливости аорты и профиля скорости антероградного и ретроградного потока, который не является уплощенным ни в дуге, ни в нисходящем отделе аорты.

Читайте также: Змз 409 клапана встречаются
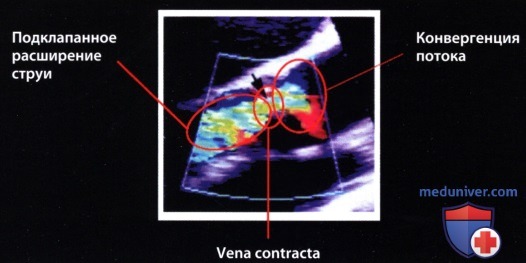
д) «Vena contracta». При аортальной недостаточности кровь из аорты забрасывается обратно в левый желудочек и достигает своей максимальной скорости в наиболее узкой части потока -на уровне так называемой эффективной площади поперечного сечения регургитации, или «vena contracta». До этого уровня поток крови ламинарный и лишь дистальнее становится турбулентным.
Эффективная площадь поперечного сечения регургитации на уровне «vena contracta» определяет объем регургитации и в принципе является наиболее информативным и наглядным параметром, характеризующим количественно аортальную недостаточность. Однако прямое измерение площади поперечного сечения на уровне «vena contracta» с помощью двумерной ЭхоКГ и цветового допплеровского картирования невозможно из-за недостаточного латерального разрешения ультразвукового луча.
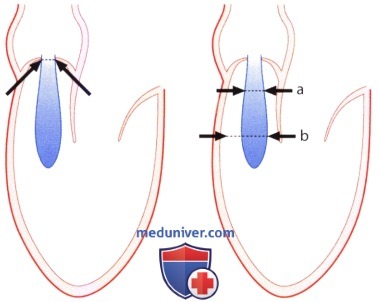
В качестве «суррогата» эффективной площади регургитации можно использовать диаметр «vena contracta», измеренный с помощью двумерной ЭхоКГ. «Vena contracta» лоцируют на уровне кольца аортального клапана вдоль длинной оси сердца из парастернальной позиции датчика. Правомочность такого способа измерения для количественной характеристики аортальной недостаточности доказана в ряде исследований. Этот способ имеет существенные преимущества перед измерением ширины струи регургитации, так как на уровне «vena contracta» ток ламинарный и условия измерения воспроизводимы. Дистальнее «vena contracta» ток становится турбулентным, поэтому на ширину струи влияет множество факторов, которые существенно снижают воспроизводимость результатов определения этого параметра. Струя регургитации из-за появляющейся турбуленции уже в проксимальном своем отделе шире, чем «vena contracta». Ширина струи регургитации, в отличие от ширины «vena contracta», зависит от настройки аппарата, гемодинамических условий и податливости принимающей камеры.
В исследовании Tribouilloy и соавт. у 79 больных с аортальной недостаточностью ширина струи регургитации составила 10±5 мм и тем самым оказалась вдвое шире, чем диаметр «vena contracta», который был равен 5±2 мм. Принципиальное различие между этими двумя параметрами представлено на рисунке ниже. Отношение ширины струи регургитации к диаметру выносящего отдела левого желудочка (граничное значение для аортальной недостаточности составляет более 40%) более предпочтительно для количественной характеристики аортальной недостаточности, чем изолированное измерение диаметра «сжатой вены». В упомянутом выше исследовании Tribouilloy и соавт. выявлена корреляция между диаметром «vena contracta» и определенной эхокардиографически площадью сжатого сечения струи регургитации. Корреляция отмечена как в отношении эксцентрической, так и концентрической струи. Гемодинамически значимую аортальную недостаточность (с выбранной для нее в качестве критерия площадью поперечного сечения струи регургитации >30 мм 2 ) при граничном значении диаметра «vena contracta» >6 мм можно было бы предсказать с чувствительностью 95% и специфичностью 90%. На рисунке ниже показана «vena contracta» у больных с легкой и тяжелой аортальной недостаточностью.
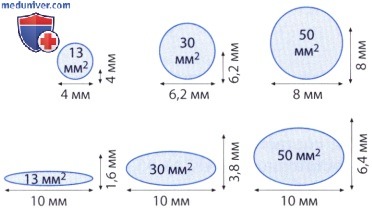
1. Ограничения данного параметра. Примерно в 30% случаев, особенно когда струя регургитации бывает множественной или эксцентричной, при двустворчатом аортальном клапане, при кальцинозе клапана и при расширении аорты может оказаться невозможно или во всяком случае трудно точно измерить диаметр «vena contracta». В таких случаях ищут альтернативные позиции для установления датчика; его, например, можно установить в парастернальную позицию справа или слева на уровне второго или третьего межреберья в положении больного на правом боку или лоцировать «vena contracta» при ЧПЭ. Наконец, следует отметить, что сжатое сечение струи регургитации лишь в очень редких случаях имеет округлую форму, и только в этих случаях можно на основании диаметра «vena contracta», измеренного с помощью двумерной ЭхоКГ, математически корректно рассчитать площадь сжатого сечения струи регургитации. При округлом сжатом сечении струи регургитации площадью 30 мм 2 диаметр «vena contracta» составляет 6,2 мм независимо от направления ультразвукового луча. При щелевидном сжатом сечении струи регургитации для такого же значения площади «сжатая вена», как показано на рисунке 17.29, в одном измерении может быть равна 3,8 мм, в другом — 10 мм. Эту особенность при измерении диаметра «vena contracta» с помощью двумерной ЭхоКГ не учитывают, что может стать причиной как заниженной, так и завышенной оценки аортальной недостаточности.
2. Новые подходы. Принципиально новый многообещающий подход для решения этой проблемы дает трехмерная реконструкция струи регургитации в области «vena contracta». Альтернативным методом является определение объема регургитируемой крови как интеграла допплеровской «мощности» (количество отражающих частиц) и умноженной на линейную скорость кровотока на уровне «vena contracta». Уже в ранее проведенных исследованиях была показана возможность определения степени регургитации по интенсивности сигнала, получаемого при непрерывноволновой допплерографии. Однако в этих исследованиях соотношение между интенсивностью сигнала и объемной скоростью существенно варьировало, так как интенсивность допплеровского сигнала отражала турбулентность всей струи регургитации в целом. Однако Buck и соавт., пользуясь в эксперименте и клинике методикой, при которой исследуют лишь ламинарный ток на уровне «сжатой вены», получили многообещающие результаты, свидетельствующие о возможности количественной оценки аортальной недостаточности.
е) Прямое определение площади поперечного сечения струи регургитации. Для того чтобы учесть неправильную конфигурацию поперечного сечения струи регургитации, появляется все больше сторонников прямой визуализации этого сечения на уровне «vena contracta» и планиметрического определения его площади. Однако следует учесть, что ламинарный поток крови на уровне «vena contracta» лоцировать в направлении, перпендикулярном направлению движения струи, невозможно. Если при цветовом допплеровском картировании удается визуализировать струю регургитации, следует, лоцируя сердце вдоль короткой оси, получить косой срез на уровне «vena contracta» или турбулентной части струи.
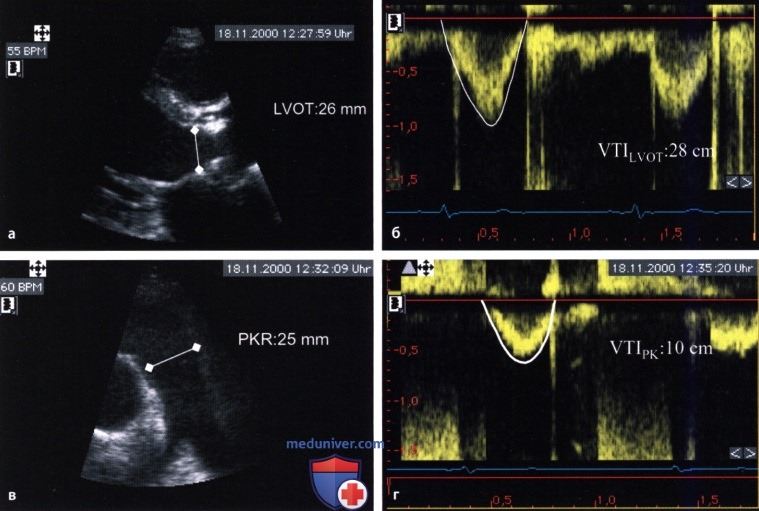
Определение фракции регургитации (ФР) у больного с тяжелой аортальной недостаточностью (IV степень):
а — Определение диаметра выносящего тракта левого желудочка (LVOT) при двухмерной ЭхоКГ.
б — Определение интеграла линейной скорости систолического трансаортального кровотока (VTILVOT).
в — Определение диаметра пульмонального клапанного кольца (PKR).
г — Определение интеграла линейной скорости систолического транспульмонального кровотока (VTIRK).
Расчет фракции аортальной регургитации (ФР):
1. Ударный объем (SVLVOT) на уровне выносящего тракта левого желудочка: SVLVOT = 1,3 2 • π • 28 = 149 мл.
2. Ударный объем на уровне пульмонального клапанного кольца: SVRK = 1,25 2 • π • 10 = 49 мл.
3. Объем регургитации: SVрег= SVLVOT— SVРК = 149-49 = 100 мл.
4. Фракция регургитации: RF = SVрег/SVLVOT= 100/149 = 0,67 = 67%.
ж) Количественное допплеровское исследование. Эффективную площадь поперечного сечения струи регургитации аналогично площади отверстия аортального клапана при его стенозе (см. выше) рассчитывают на основании уравнения непрерывности потока.
1. Объем регургитации (SVрег). Объем регургитации вычисляют как разницу между общим объемом крови, протекающей через аортальный клапан во время систолы SVtotal и эффективным ударным объемом SVeff:
2. Общий объем крови SVtotal. Для измерения общего объема крови SVtotal существуют два метода:
Читайте также: Воздушный фильтр с обратным клапаном
— Определение ударного объема в выносящем тракте левого желудочка.
— Волюметрическое определение ударного объема левого желудочка по модифицированному методу Симпсона.
3. Эффективный ударный объем SVeff. Эффективный ударный объем крови SVeff определяют:
— либо на клапане легочной артерии,
— либо на митральном клапане.
Ударный объем, определенный на клапане легочной артерии и на митральном клапане, соответствует произведению площади отверстия соответствующих клапанов на интеграл линейной скорости, измеренной с помощью допплерографии. На точность определения ударного объема особенно сильно влияет измерение диаметра клапанного кольца, так как в формуле для определения ударного объема значение диаметра возводят в квадрат. При измерении диаметра клапанного кольца легочной артерии, которое осуществляют обычно, лоцируя его вдоль короткой оси из парастернальной позиции, латеральный край кольца виден нечетко. Определение ударного объема на митральном клапане также сопряжено с трудностями при измерении митрального кольца. Митральное кольцо имеет эллиптическую форму, поэтому площадь отверстия митрального клапана рассчитывают, используя значение двух осей эллипса, измеренных в плоскости четырех камер (d4K) и в плоскости двух желудочков (d2K): площадь отверстия митрального клапана SMK = d4K * d2K * π/4.
Этот метод трудоемкий, и, кроме того, при измерении размеров клапана ультразвуковой датчик далеко отстоит от клапанного кольца, а латеральное разрешение ультразвукового луча недостаточное. Наконец, использовать данный метод в тех случаях, когда имеется митральная недостаточность, невозможно. Учитывая перечисленные выше недостатки метода измерения размеров митрального клапанного кольца, мы предпочитаем определять ударный объем на клапане легочной артерии.
4. Фракция регургитации RFAO. Фракцию регургитации определяют как отношение объема регургитации к общему объему выбрасываемой крови:
При фракции регургитации менее 30% говорят о легкой аортальной недостаточности (AI 1+). Фракция регургитации, равная 30-45%, соответствует умеренной аортальной недостаточности (AI 2+), 45-60% — тяжелой (AI 3+), более 60% — очень тяжелой (AI 4+).
5. Эффективная площадь поперечного сечения струи регургитации (ЭПР). Эффективную площадь поперечного сечения струи регургитации, как было упомянуто выше, рассчитывают в соответствии с уравнением непрерывности потока на основании объема регургитации SVрег и интеграла линейной скорости струи регургитации (VTIрег), измеренных с помощью непрерывноволновой допплерографии:
Этот параметр, по сравнению с объемом регургитации и фракцией регургитации, в меньшей степени зависит от пред- и постнагрузки левого желудочка.
6. Граничные значения. Для гемодинамически значимой аортальной недостаточности выведены следующие граничные значения: площадь поперечного сечения струи регургитации более 30 мм 2 , объем регургитации более 60 мл и фракция регургитации более 45%.
7. Значение количественного допплеровского исследования. Описанные методики расчета гемодинамических параметров с помощью допплеровского исследования очень трудоемкие и требуют от исследователя большого опыта. Многочисленные измерения, которые приходится выполнять, становятся причиной ошибок и снижают воспроизводимость результатов. Как и в случае других сложных параметров, параметры, которые были здесь рассчитаны, лишь тогда могут найти широкое применение в клинической практике, когда более простые показатели, на которых они основываются, удастся точно определить.
д) Конвергенция проксимальной части потока. Концепция «конвергенции проксимальной части потока» (Proximal Isovelocity Surface Area — PISA), разработанная для количественной оценки клапанной недостаточности, основывается на феномене, суть которого сводится к тому, что кровь, протекая через отверстие несостоятельного клапана, ускоряется в так называемой зоне конвергенции. В этой зоне все клетки крови, движущиеся с одинаковой скоростью, распределяются по условной полусферической поверхности, центр которой находится в регургитационном отверстии. Зона конвергенции формируется из многочисленных концентрических полусфер, окружающих регургитационное отверстие. В принципе, согласно уравнению непрерывности потока, объемная скорость потока, рассчитываемая как произведение площади поверхности полусферического слоя на линейную скорость кровотока, для разных слоев одинакова. Чем меньше радиус полусферы, тем выше линейная скорость на ее поверхности. С помощью цветового допплеровского картирования можно «окрасить» полусферические слои соответственно предельной скорости Найквиста в разные цвета на допплеровском изображении.
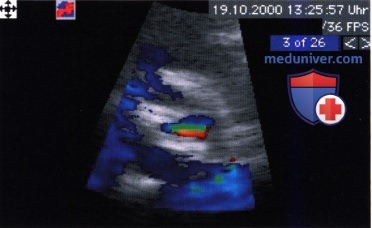
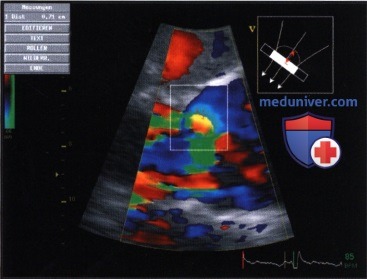
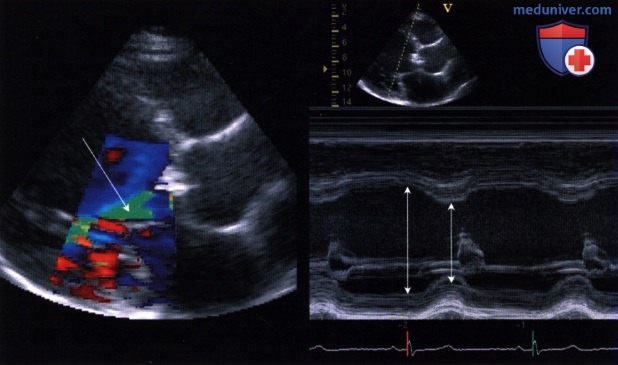
На рисунке ниже показана зона конвергенции, зарегистрированная у больного с гемодинамически значимой аортальной недостаточностью. Зная заданный предел Найквиста V (в нашем случае он равен 69 см/с) и радиус r полусферы в середине диастолы (равен расстоянию от зон, окрашенных в разный цвет, до регургитационного отверстия — в данном случае 0,71 см), можно рассчитать объем регургитации Q:
Q (мл/с) = 2π х r 2 • V = 2л • 0,71 2 см/с = 218 мл/с.
Зная объем регургитации Q и определив путем перемещения датчика в апикальную позицию среднюю линейную скорость струи регургитации, можно рассчитать эффективную площадь поперечного сечения струи регургитации (А):
А = Объем регургитации/Средняя линейная скорость струи регургитации в диастолу = 218/300 = 0,72 см 2 .
Недостатки метода. Следует отметить следующие недостатки концепции конвергенции проксимальной части струи:
— Участки струи с одинаковой линейной скоростью часто образуют не полусферы, а чашеобразные оболочки, имеющие разную ширину и высоту.
— Регургитационное отверстие при аортальной недостаточности часто имеет не округлую форму, которая необходима для расчетов в соответствии с концепцией конвергенции проксимальной части потока, а приобретает весьма сложную конфигурацию из-за изменений, обусловленных эндокардитом или пролапсом створок аортального клапана.
— Обызвествление аортального клапана и стенки аорты влияют на геометрию зоны конвергенции.
— Аорта препятствует латеральному отклонению зоны конвергенции, что может привести к завышенным значениям объема регургитации.
В целом, валидность метода, основанного на концепции конвергенции проксимальной части потока при количественной оценке аортальной недостаточности, пока окончательно не доказана, и поэтому он не получил широкого применения. Его можно использовать наряду с другими методами при определении степени тяжести аортальной недостаточности: минимальная или слабая конвергенция струи регургитации через аортальный клапан говорит о легкой аортальной недостаточности, в то время как выраженная конвергенция соответствует тяжелой аортальной недостаточности. При ортогональном расположении зоны конвергенции относительно направления лоцирования можно воспользоваться приведенными в работе Giesler и соавт. критериями тяжелой аортальной недостаточности (PISA-радиус >0,7 см при пределе Найквиста не менее 30 см/с).
е) Заключение. Описанные методы из-за перечисленных недостатков по своей диагностической ценности ограничены, поэтому часто бывает целесообразно для повышения достоверности диагноза применять их вместе. Если при использовании двух методов получают примерно одинаковую количественную оценку степени тяжести, то ее можно считать достоверной. Так, о легкой аортальной недостаточности можно говорить в том случае, когда при лоцировании в плоскости четырех камер из апикальной позиции датчика выявляют цветную струю лишь в непосредственной близости от клапана и одновременно преимущественно антероградный кровоток в грудной аорте во время диастолы.
О тяжелой аортальной недостаточности говорят в том случае, если ширина струи регургитации на уровне «vena contracta» равна 7 мм и более, а РНТ (Т1/2P)
🎬 Видео
Эхокардиография в диагностике и ведении пороков аортального клапана сердцаСкачать

Болезни аортального клапана: аортальный стеноз, недостаточность аортального клапана.Скачать

УЗИ сердца. Двустворчатый аортальный клапан и еще одна аномалия...Скачать

Двустворчатый аортальный клапан и локальные нарушения сократимости левого желудочкаСкачать

Двухстворчатый аортальный клапанСкачать

Детская Эхокардиография (УЗИ сердца) - Бикуспидальный аортальный клапан с регургитацией у подросткаСкачать

Детская Эхокардиография (УЗИ сердца) - Двустворчатый (бикуспидальный) аортальный клапан у ребенкаСкачать

Двухстворчатый аортальный клапан и физическая активностьСкачать

Тяжелая недостаточность двустворчатого аортального клапана на фоне инфекционного эндокрадитаСкачать

Аортальный порок. Что может современная хирургия?Скачать

Двустворчатый аортальный клапанСкачать

Двустворчатый клапан, парастернальный доступ по длинной осиСкачать

Двухстворчатый аортальный клапанСкачать

Недостаточность аортального клапана.Скачать

ЭхоКГ в оценке функции протезированных клапанов сердца и диагностике осложнений протезированияСкачать

Пролапс митрального клапана? Двустворчатый аортальный клапан. Уа 17 лет. Хочет в ВДВ, пустят?Скачать

УЗИ сердца в 19 лет. Что с аортальным клапаном?Скачать

Протезирование аортального клапанаСкачать