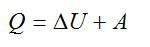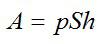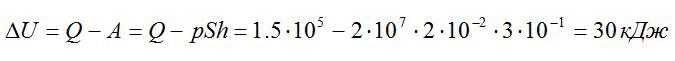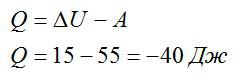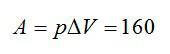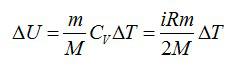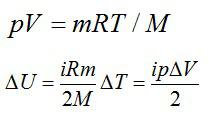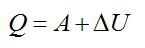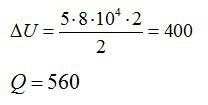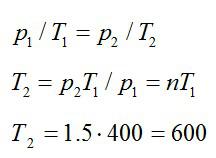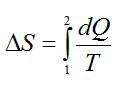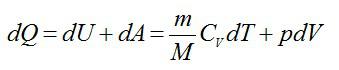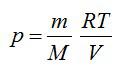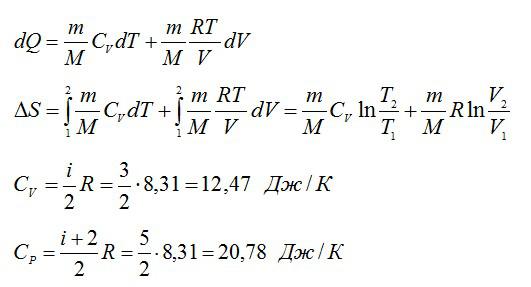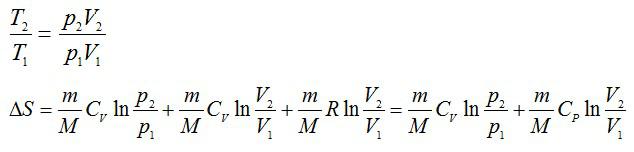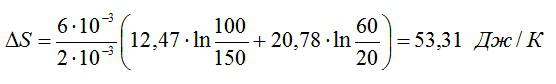Первый закон, или первое начало термодинамики является частным случаем закона сохранения энергии. Разберемся, как он работает, с помощью решения простых задач. Кстати, у нас есть и примеры решения задач на второе начало термодинамики.
Подписывайтесь на наш телеграм-канал, чтобы не только легко решать задачи, но и узнавать лайфхаки для любых жизненных ситуаций.
- Первый закон термодинамики: решение задач
- Задача №1. Применение первого закона термодинамики
- Задача №2. Применение первого закона термодинамики
- Задача №3. Расчет работы, изменения внутренней энергии и количества теплоты
- Задача №4. Изопроцессы
- Задача №5. Расчет изменения энтропии
- Вопросы по теме «1-ый закон термодинамики»
- Идеальному газу находящемуся в цилиндре с поршнем сообщили количество теплоты
- Идеальному газу находящемуся в цилиндре с поршнем сообщили количество теплоты
- Идеальному газу находящемуся в цилиндре с поршнем сообщили количество теплоты
Первый закон термодинамики: решение задач
Алгоритм решения задач на первый закон термодинамики ничем не отличается от алгоритма решения любой другой физической задачи. С ним вы можете ознакомиться, открыв нашу универсальную памятку. Также полезно будет держать под рукой формулы, которые часто используются при решении задач.
Задача №1. Применение первого закона термодинамики
Газ находился в цилиндре с поршнем площадью поперечного сечения 200 см^2. После того, как газ нагрели, сообщив ему количество теплоты в 1,5*10^5 Дж, поршень сдвинулся на расстояние h=30 см. Как изменилась внутренняя энергия газа, если его давление осталось равным 2*10^7 Па.
Запишем первое начало термодинамики:
Работу против внешних сил, которую совершил газ, можно найти по формуле из механики:
Ответ: 30 кДж.
Задача №2. Применение первого закона термодинамики
Над газом была совершена работа 55 Дж, а его внутренняя энергия увеличилась на 15 Джоулей. Какое количество теплоты получил или отдал газ в этом процессе?
Записываем первое начало термодинамики и подставляем значения:
A пишется со знаком «минус», так как это работа внешних сил над газом, а не наоборот.
Ответ: в процессе газ отдал 40 Дж теплоты.
Задача №3. Расчет работы, изменения внутренней энергии и количества теплоты
Кислород нагрели при постоянном давлении p=80 кПа. Объем газа увеличился с 1 до 3 кубических метров. Определить изменение внутренней энергии кислорода, работу, совершенную газом, и количество теплоты, сообщенное ему.
Изменение внутренней энергии равно:
Используем уравнение состояния газа:
Число степеней свободы i для двухатомной молекулы равно 5.
Согласно первому закону термодинамики, сообщенное газу тепло равно:
Ответ: А=160 кДж, ∆U=400 кДж, Q=560 кДж.
Задача №4. Изопроцессы
Газ находится в баллоне при температуре 400 К. До какой температуры нужно нагреть газ, чтобы его давление увеличилось в 1,5 раза?
Читайте также: Рабочий цилиндр сцепления блейзер шевроле
Так как нагревание газа происходит при постоянном объеме, процесс – изохорный. При изохорном процессе:
Ответ: 600 К.
Задача №5. Расчет изменения энтропии
Найти изменение ∆S энтропии при расширении массы m = 6 г гелия от объема V1 = 20 л под давлением р1 = 150 кПа к объему V2 = 60 л под давлением р2 = 100 кПа.
Изменение энтропии при переходе вещества из состояния 1 в состояние 2:
Согласно первому началу термодинамики:
Из уравнения Менделеева-Клапейрона выразим давление:
Из уравнения Менделеева-Клапейрона:
Кстати! Для наших читателей действует скидка 10% на любой вид работы.
Вопросы по теме «1-ый закон термодинамики»
Вопрос 1. Приведите пример действия первого закона термодинамики.
Ответ. В качестве примера можно привести газ в сосуде. Если сообщить ему какое-то количество теплоты, оно пойдет на увеличение внутренней энергии газа в сосуде.
Вопрос 2. Сформулируйте первый закон термодинамики.
Ответ. В любой изолированной системе запас энергии остается постоянным.
Вопрос 3. Как еще можно сформулировать первый закон термодинамики?
Ответ. Вот разные формулировки первого закона термодинамики:
- Количество теплоты, полученное системой, идет на изменение внутренней энергии системы, а также на совершение работы против внешних сил.
- Невозможен вечный двигатель первого рода (двигатель, совершающий работу без затраты энергии).
Вопрос 4. Что такое изопроцесс? Какие есть изопроцессы?
Изопроцесс – это термодинамический процесс, при котором один из параметров системы (давление, объем, температура, энтропия) остается неизменным.
- изотермическим (T=const);
- изобарным (P=const);
- изохорным (V=const);
- Адиабатическим (отсутствует теплообмен с окружающей средой).
Вопрос 5. При каком изопроцессе газ не совершает работу?
Ответ. При изохорном.
Ищете, где почитать теорию по теме, а учебника нет под рукой? Далеко ходить на надо, почитайте наш отдельный материал по первому началу термодинамики. А если при решении заданий понадобится помощь, обращайтесь в профессиональный студенческий сервис.
Иван Колобков, известный также как Джони. Маркетолог, аналитик и копирайтер компании Zaochnik. Подающий надежды молодой писатель. Питает любовь к физике, раритетным вещам и творчеству Ч. Буковски.
Идеальному газу находящемуся в цилиндре с поршнем сообщили количество теплоты
Систему отсчета, связанную с Землей, будем считать инерциальной. В процессе медленного подъема поршня его ускорение считаем ничтожно малым. Поэтому сумма приложенных к поршню сил при его движении равна нулю. В проекциях на вертикальную ось у получаем: \( — — Mg = 0 \), или \(
Отсюда получаем давление газа \( p \), под движущимся поршнем: \(
+ \frac > \). Используем модель одноатомного идеального газа: \( \left\ pV = vRT\\ U = \frac vRT \end \right. \)
Читайте также: Камминз зазор поршень цилиндр
Отсюда получаем: \( U = \frac pV \)
Внутренняя энергия газа в исходном состоянии \( = \frac
Sh \), а в конечном состоянии
Процесс движения поршня идет при постоянном давлении газа \(
\) Поэтому из первого начала термодинамики получаем: \( Q = — +
Подставляя сюда выражения для \(
\), \( \) и \( \), получим: \( Q = \frac (
S + Mg)(H — h) = \) \( \frac Mgh + \frac (Mg +
Ответ: \( \frac Mgh + \frac (Mg +
Идеальному газу находящемуся в цилиндре с поршнем сообщили количество теплоты
В гладком вертикальном цилиндре под подвижным поршнем массой M = 5 кг и площадью S = 100 см 2 находится идеальный одноатомный газ. После сообщения газу некоторого количества теплоты поршень приподнялся на высоту Δh = 5 см над дном цилиндра, а газ нагрелся на ΔT = 30 К. Найдите удельную теплоёмкость газа в данном процессе. Давление в окружающей цилиндр среде равно p0 = 10 4 Па, масса газа в цилиндре m = 0,12 г.
Как следует из условия, объём газа равен а давление равно в течение всего процесса подвода теплоты. Согласно уравнению Клапейрона — Менделеева где — количество газа (в молях). Отсюда В процессе подвода теплоты в изобарическом процессе будет выполняться соотношение: так что После сообщения газу некоторого количества теплоты температура газа увеличилась на а поршень приподнялся на высоту причём согласно первому началу термодинамики где изменение внутренней энергии для одноатомного идеального газа а работа газа в изобарическом процессе
Таким образом, а удельная теплоёмкость газа в данном изобарическом процессе равна по определению:
I) записаны положения теории и физические законы, закономерности, применение которых необходимо для решения задачи выбранным способом ((в данном случае — определение удельной теплоёмкости, уравнение Клапейрона—Менделеева, первое начало термодинамики, выражения для внутренней энергии идеального одноатомного газа и для работы газа при изобарическом процессе);
II) описаны все вновь вводимые в решении буквенные обозначения физических величин (за исключением обозначений констант, указанных в варианте КИМ, и обозначений величин, используемых в условии задачи);
III) проведены необходимые математические преобразования, приводящие к правильному ответу;
Записи, соответствующие пункту II, представлены не в полном объёме или отсутствуют.
Лишние записи, не входящие в решение (возможно, неверные), не отделены от решения (не зачёркнуты, не заключены в скобки, рамку и т. п.).
В необходимых математических преобразованиях или вычислениях допущены ошибки, и (или) преобразования/вычисления не доведены до конца.
Представлены только положения и формулы, выражающие физические законы, применение которых необходимо для решения задачи, без каких-либо преобразований с их использованием, направленных на решение задачи, и ответа.
В решении отсутствует одна из исходных формул, необходимая для решения задачи (или утверждение, лежащее в основе решения), но присутствуют логически верные преобразования с имеющимися формулами, направленные на решение задачи.
Количество теплоты переданное газу равна изменению внутренней энергии + работе газа+работе силы тяжести. При сложении работы газа и внутренней энергии получаем 5/2, но у вас 5/2 умножается еще и на работу силы тяжести. Я думаю 5/2 должно быть внутри скобки перед роS
Смотрите решение. То, про что Вы говорите, это не работа силы тяжести.
Идеальному газу находящемуся в цилиндре с поршнем сообщили количество теплоты
Систему отсчета, связанную с Землей, будем считать инерциальной. В процессе медленного подъема поршня его ускорение считаем ничтожно малым. Поэтому сумма приложенных к поршню сил при его движении равна нулю. В проекциях на вертикальную ось у получаем: \( — — Mg = 0 \), или \(
Отсюда получаем давление газа \( p \), под движущимся поршнем: \(
+ \frac > \). Используем модель одноатомного идеального газа: \( \left\ pV = vRT\\ U = \frac vRT \end \right. \)
Отсюда получаем: \( U = \frac pV \)
Внутренняя энергия газа в исходном состоянии \( = \frac
Sh \), а в конечном состоянии
Процесс движения поршня идет при постоянном давлении газа \(
\) Поэтому из первого начала термодинамики получаем: \( Q = — +
Подставляя сюда выражения для \(
\), \( \) и \( \), получим: \( Q = \frac (
S + Mg)(H — h) = \) \( \frac Mgh + \frac (Mg +
Ответ: \( \frac Mgh + \frac (Mg +