- Эндоваскулярное протезирование аортального клапана (TAVI)
- Причины аортального порока
- Как выполняется протезирование аортального клапана в клинике ЦЭЛТ?
- Каковы преимущества транскатетерной имплантации аортального клапана перед открытой операцией?
- Миниинвазивные операции протезирования клапана аорты
- Имплантация протеза аортального клапана
- Материал и методы
- Обсуждение
- Заключение
- 🔥 Видео
Видео:Протезирование аортального клапанаСкачать

Эндоваскулярное протезирование аортального клапана (TAVI)
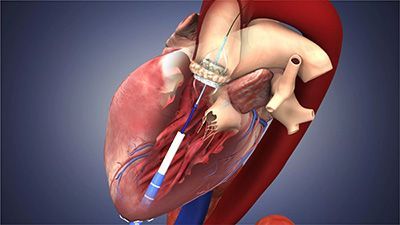
Транскатетерное эндоваскулярное (внутрисосудистое) протезирование аортального клапана (также — транскатетерная имплантация аортального клапана или TAVI) — это процедура замены аортального клапана при его критическом стенозе (сужении) доступом через бедренную артерию под местной анестезией.
При нормально функционировании, обогащённая кислородом и питательными веществами кровь из сердца поступает в аорту, откуда по ветвям аорты (артериям) кислород доставляется всем органам и тканям. Аортальный клапан находится на выходе из сердца и обеспечивает кровоток только в одном направлении — от сердца к аорте. Сужение, или стеноз аортального клапана приводит к значительному затруднению работы сердца. Известные на сегодняшний день статистические данные говорят о том, что без проведения операции средняя ежегодная летальность больных с симптомами аортального порока составляет около 10%.
операция, пребывание в стационаре, послеоперационное наблюдение лечащим врачом, медикаменты и питание
- острые инфекционные заболевания;
- выраженные нарушения свертывающей системы крови;
- невозможность применения кровьразжижающих препаратов.
Видео:Эндоваскулярное протезирование аортального клапана.Скачать

Причины аортального порока
Существует множество патологических состояний, которые со временем могут приводить к дегенеративным изменениям, отложению кальция на створках аортального клапана, изменению его функции.
Сердце человека способно некоторое время компенсировать нарушение кровообращения. Рано или поздно возникают клинические проявления: головокружение, одышка, обмороки, сердцебиение, синдром стенокардии. Консервативно (с помощью медикаментов) можно частично компенсировать состояние пациента, но не изменить его кардинально и не улучшит качество жизни..
Видео:TAVI - Transcatheter Aortic Valve Implantation/Транскатетерная имплантация аортального клапанаСкачать

Как выполняется протезирование аортального клапана в клинике ЦЭЛТ?
Эффективный метод лечения аортального порока — замена клапана искусственным биологическим протезом. Существует два способа такой операции – традиционный хирургический и эндоваскулярный (без разрезов грудной клетки).
Традиционно операция по замене аортального клапана уже многие годы выполняется открытым способом — то есть через вскрытие грудной полости. Операция проводится с исключением сердца пациента из системы кровообращения и использованием аппарата искусственного кровообращения (АИК). Однако технологии в медицине не стоят на месте. Несколько лет назад появилась новейшая малоинвазивная методика — транскатетерная имплантация аортального клапана (TAVI). В ряде случаев пациенту возможно выполнить протезирование аортального клапана именно таким способом.
Принцип операции эндоваскулярного протезирования аортального клапана похож на операции по стентированию и состоит в том, что доступом через бедренную артерию к месту поврежденного аортального клапана подводится специальный катетер с размещенным на его конце искусственным клапаном (биопротезом) в сложенном виде. Перед установкой этого искусственного клапана производят расширение просвета собственного аортального клапана с помощью специального баллона. Биопротез для TAVI представляет собой специально обработанный трехстворчатый клапан из бычьего перикарда, закрепленный в стенте (металлическом каркасе). Операция для пациента безболезненна, так как выполняется под наркозом. Существует два вида клапанов: баллон расправляющийся и саморасправляющийся.
Обычно TAVI выбирается в качестве метода лечения пациентов старше 75 лет с тяжелым аортальным стенозом, имеющих противопоказания к проведению открытой хирургической операции, но на сегодняшний день показания расширены и для пациентов с низким и средним хирургическим риском.
Видео:Протезирование аортального и митрального клапанов при инфекционном эндокардитеСкачать

Каковы преимущества транскатетерной имплантации аортального клапана перед открытой операцией?
При внутрисосудистом протезировании аортального клапана отсутствуют большие разрезы, что значительно сокращает длительность послеоперационной реабилитации, уменьшает болевой синдром и исключает развитие осложнений, связанных с воспалением (нагноением) послеоперационных швов. К другим важным преимуществам TAVI можно отнести:
- Возможность выполнять операцию пациентам с высоким хирургическим риском, пожилым пациентам и пациентам с тяжелыми сопутствующими заболеваниями
- Небольшая продолжительность операции, уменьшенные операционные травмы.
- Операция проводится под местной анестезией (в некоторых случаях под наркозом)
- Отсутствие необходимости подключения к аппарату искусственного кровообращения и «выключения» сердца пациента
- Сокращение сроков нахождения в стационаре
- Низкий процент послеоперационных осложнений и быстрая адаптации после выписки из стационара
Видео:ЭхоКГ в оценке функции протезированных клапанов сердца и диагностике осложнений протезированияСкачать

Миниинвазивные операции протезирования клапана аорты
Кровь, изгоняемая сердцем, попадает в аорту. Аорта – это самый большой сосуд в организме человека, через который кровь направляется к органам и тканям. Аорта соединяется с сердцем при помощи клапана аорты. Открываясь, этот клапан способствует оттоку крови от сердца, закрываясь, он препятствует проникновению крови обратно в сердечные камеры.
Операция по замене (протезированию) клапана аорты может потребоваться в случае возникновения дисфункции (неисправности) клапана. Это, в свою очередь, может быть обусловлено двумя причинами:
- Клапан аорты сужается и не пропускает требуемое количество крови, т.е. поступление крови к организму снижается – это называется «аортальный стеноз». Среди основных причин выделяют возрастные дегенеративные изменения и ревматизм.
- Клапан «протекает», не удерживает кровь, и кровь проникает обратно в полость сердца – это называется «аортальная недостаточность». Основные причины: врождённые генетические дефекты, возрастное расширение аорты и клапанного кольца, заболевания аорты и бактериальное поражение клапана.
Операция протезирования клапана аорты подразумевает удаление вышедшего из строя клапана и замену его на искусственный. Операция выполняется в условиях искусственного кровообращения, т.е. на остановленном сердце, когда функцию кровоснабжения органов и тканей перенимает на себя специальный аппарат. Во время операции пациент находится в состоянии наркоза и не чувствует боли.
Впервые операция протезирования клапана аорты на искусственный клапан была выполнена в начале 1960 годов. Традиционно, операция выполняется через срединный разрез в области грудины длиной 20 см. Для того, чтобы достичь сердца, необходимо рассечь кожу, мягкие ткани, кость, расположенную в середине груди, именуемую грудиной, и специальную сердечную оболочку – перикард. Следующим этапом производится подключение аппарата искусственного кровообращения путём последовательного соединения с ним аорты и сердечных вен, а затем временная остановка сердца. Дальше, хирург рассекает аорту в поперечном направлении, чтобы увидеть аортальный клапан. Если клапан сильно повреждён, он удаляется, и на его место вшивается новый, искусственный клапан сердца. Искусственные клапаны делятся на два вида:
- Механический (металло-углеродный): долговечен, может эффективно работать десятилетиями, но требует пожизненного приёма препаратов, снижающих свёртываемость крови (антикоагулянтов), что повышает риск кровотечения;
- Биологический (созданный из ткани животных или человека): более физиологичен, но менее долговечен, служит не более 20 лет, но не требует пожизненного приёма антикоагулянтов.
 | 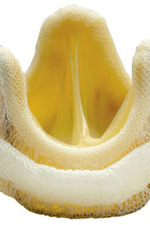 |
| Современные виды искусственных клапанов сердца: слева – механический; справа – биологический. | |
После установки нового клапана по очереди восстанавливается целостность аорты, грудины, мягких тканей груди и кожи. По продолжительности операция занимает 2,5 – 3 часа.
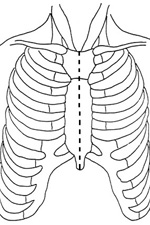 | 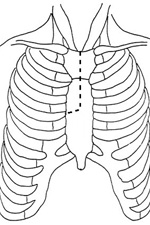 |
| Схема операционного доступа. Полная срединная стернотомия (слева), J-образная министернотомия (справа). | |
Современные знания и опыт позволяют уменьшить размер раны груди для выполнения операции по замене клапана аорты. Такие операции носят название миниинвазивных, т.е. малотравматичных – через уменьшенный доступ. Использование малых доступов было предложено в середине 1990-х годов.
Читайте также: Распиновка датчиков ваз 2114 инжектор 8 клапанов
Техника оперативного вмешательства остаётся прежней, но при этом длина разреза всего 7 сантиметров, и можно обойтись без полного рассечения грудины (полной срединной стернотомии), что позволяет значительно снизить травматичность операции, выраженность боли в послеоперационном периоде, сохранить каркасную функцию грудной клетки, ускорить восстановление дыхательной функции и возвращение к привычной жизни при сохранении высокой эффективности лечения.
Несомненным достоинством для пациента при этой операции является косметический результат.
В отличие от традиционной операции миниинвазивные операции занимают несколько больше времени (3 – 3,5 часа).
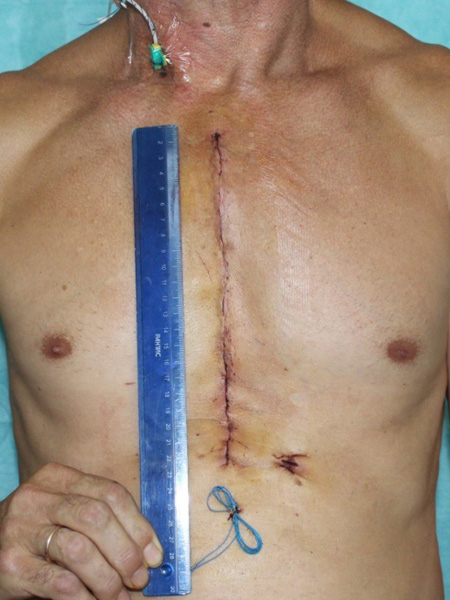 | 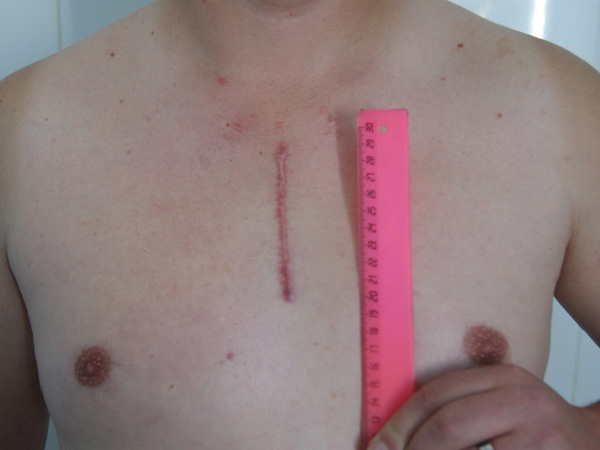 |
Рис. 3. Внешний вид раны грудипосле традиционной (слева) и миниинвазивной операции (справа).
В течение последнего десятилетия был разработан новый, уникальный способ замены клапана аорты: операция транскатетерной имплантации аортального клапана (Transcatheter Aortic Valve Implantation или TAVI).
Эта процедура выполняются в условиях рентгеноперационной при участи команды, состоящей из кардиологов, кардиохирургов, специалистов по рентген-хирургии. Что особо важно, эта процедура выполняется на работающем сердце, таким образом предотвращаются риски, связанные с проведением искусственного кровообращения.
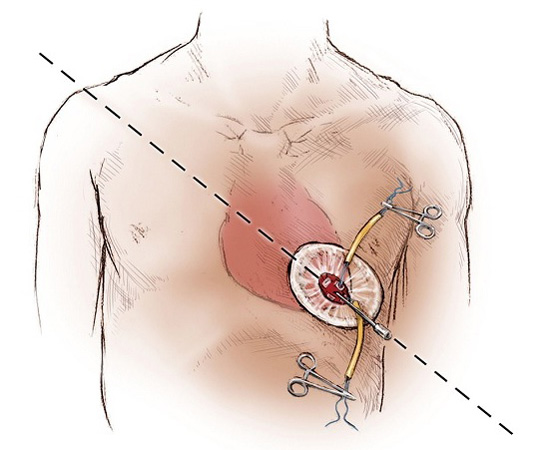
Разрез, длиной 3 см выполняется сбоку на груди так, как показано на рисунке 4. В этом случае вмешательство носит название трансапикальной катетерной имплантации клапана.
Рис. 4. Схема доступа для операции трансапикальной катетерной имплантации клапана аорты (Cheung, Lichtenstein, Annals of Cardiothoracic Surgery, 2012).
На область возле верхушки сердца накладывается два специальных кровоостанавливающих шва, через которые проводится высокотехнологичное устройство – доставочная система, диаметр которой составляет всего 8 мм. Эта система содержит биологический клапан в «свёрнутом» состоянии.
Производится позиционирование клапана на требуемом уровне под контролем рентгеновского аппарата, который может вращаться вокруг пациента на специальной дуге, благодаря чему можно получить рентгеновские снимки с различных ракурсов.
Далее искусственный клапан раскрывается, занимая заданное положение в корне аорты. Раскрытие клапана может производиться как при помощи баллона, надуваемого гелием (см. рис. 5), так и самостоятельно – у клапанов с каркасом из металла с памятью формы, именуемого «Нитинол» (сплава никеля и титана).
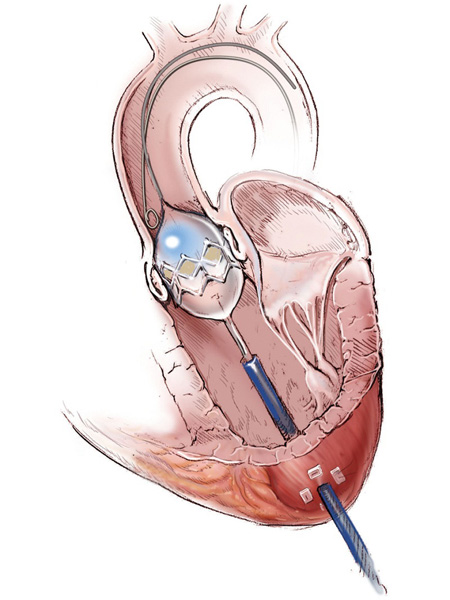 | 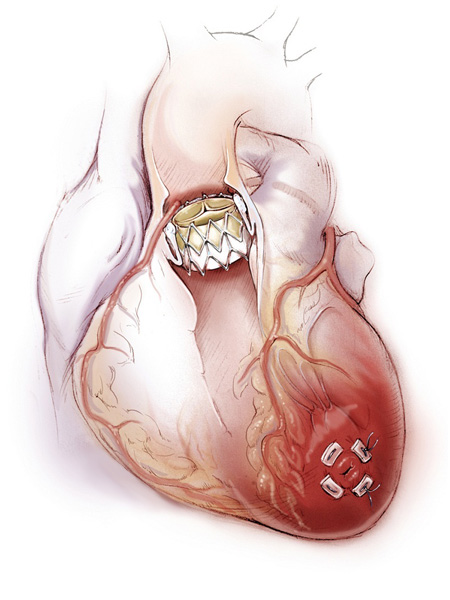 |
| Раскрытие искусственного клапана при помощи баллона | Вид клапана, установленного в аортальную позицию при трансапикальной катетерной имплантации |
| (Cheung, Lichtenstein, Annals of Cardiothoracic Surgery, 2012). | |
Рис. 6. Биологический клапан для имплантации в аортальную позицию
транскатетерным способом.
Следует однако заметить, что к проведению такой операции существуют строгие показания. Транскатетерная имплантация клапана выполняется тем пациентам, кому противопоказано традиционное оперативное вмешательство ввиду высокого риска (могут не перенести традиционную операцию): это пациенты с критическим стенозом клапана аорты, как правило, пожилые (старше 80 лет), пациенты, перенесшие операцию коронарного шунтирования, пациенты с заболеваниями аорты, которые создают технические трудности при выполнении доступа к сердцу и клапану из классического доступа.
Операция транскатетерной имплантации занимает около 40 — 60 минут, и период восстановительного лечения после неё значительно короче, по сравнению с традиционной операцией.
На отделении кардиохирургии Городской больницы №40 применяются все рассмотренные виды коррекции приобретённых пороков клапана аорты.
Видео:Операция Дэвида - реимплантация аортального клапана в протез восходящей аорты (для профессионалов)Скачать

Имплантация протеза аортального клапана
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Трансапикальная транскатетерная имплантация аортального клапана
Журнал: Кардиология и сердечно-сосудистая хирургия. 2015;8(4): 56-60
Баяндин Н. Л., Кротовский А. Г., Филатов А. А., Клыков Л. Л., Сетынь Т. В., Харламова И. Е. Трансапикальная транскатетерная имплантация аортального клапана. Кардиология и сердечно-сосудистая хирургия. 2015;8(4):56-60.
Bayandin N L, Krotovskiy A G, Filatov A A, Klykov L L, Setyn’ T V, Kharlamova I E. Transapical aortic valve implantation. Kardiologiya i Serdechno-Sosudistaya Khirurgiya. 2015;8(4):56-60.
https://doi.org/10.17116/kardio20158456-60
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Цель. Анализ результатов первого опыта применения транскатетерной имплантации аортального клапана (ТИАК) на базе городской больницы. Материал и методы. Клинический материал составили 12 пациентов, оперированных в ГКБ №15. Средний возраст — 73,9 (59—81) года, мужчин — 8, женщин — 4. Отбор пациентов проводили по следующим критериям: кальцинированный аортальный клапан (кальциноз 3-й степени) с преобладанием стеноза, высокий риск традиционного оперативного вмешательства при EuroSCORE более 20%, размер фиброзного кольца (ФК) аортального клапана (АК) — 22,5—25 мм, при гемодинамически незначимом поражении коронарных артерий и отсутствии другой значимой патологии сердца и аорты. Результаты. По данным ЭхоКГ, градиент систолического давления колебался от 53 до 138 мм рт.ст., в среднем составил 86±11 мм рт.ст. Диаметр ФК АК — от 22,5 до 25 мм. Площадь отверстия АК — от 0,6 до 0,9 см², в среднем 0,72±0,2 см². У всех пациентов был трехстворчатый аортальный клапан. В 7 случаях выполняли ТИАК трансапикальным доступом (ТАД), учитывая поражение подвздошно-бедренного сегмента артерий. Всем пациентам установлен бескаркасный протез аортального клапана Edwards Sapien. В ближайшем послеоперационном периоде наблюдали один летальный исход в связи с обтурацией протезом левой коронарной артерии.
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Городская клиническая больница №15 им. О.М. Филатова, Москва, Россия
Аортальный стеноз (АС) по-прежнему остается наиболее часто встречающейся формой приобретенного порока сердца у взрослых, частота данной патологии увеличивается с возрастом пациентов [1]. J. Ross и E. Braunwald [2] выявили, что при естественном течении клинически значимого АС прогноз неблагоприятный. У пациентов, получающих медикаментозное лечение по поводу АС с клиническими симптомами, выживаемость в течение 1 года и 5 лет составляет 60 и 32% соответственно [3]. Протезирование аортального клапана (ПАК) является единственным эффективным методом лечения больных с клиническими проявлениями А.С. Операционная летальность и частота послеоперационных осложнений у данной категории больных значительно возрастает с возрастом. Транскатетерная имплантация аортального клапана (ТИАК) открыла новые возможности в лечении пациентов, которым не была оказана помощь ввиду того, что вероятность операционной смертности превышала возможную выгоду от проведения традиционной ПАК.
При лечении пациентов, у которых диаметр бедренных артерий менее 7 мм, наблюдалась извитость подвздошных артерий и наличие кальция в сосудах, предложено использовать трансапикальный доступ (TA). Первоначальный опыт, полученный на моделях с использованием животных, применен на человеке и ранние результаты оказались многообещающими [17, 18]. Первые из опубликованных данных касались ТА и принадлежат S. Lichtenstein и соавт. [17], которые провели ТИАК 7 пациентам с АС с высокой степенью риска. Имплантация клапана была успешной у всех пациентов (не отмечено случаев смерти в ходе выполнения процедуры). Градиент на АК и улучшение состояния наблюдались у всех пациентов, при этом достигнутые результаты соотносились с показателями, получаемыми при ретроградной имплантации клапана.
Читайте также: Рено 16 клапанов ремень генератора схема
Видео:Вопросы врачу. TAVI (транскатетерная имплантация аортального клапана)Скачать

Материал и методы
Клинический материал составили 12 пациентов, оперированных в ГКБ № 15. Средний возраст больных — 73,9 (59—81) года, мужчин — 8, женщин — 4. Все пациенты предъявляли жалобы на одышку при незначительной физической нагрузке, 4 отмечали боли по типу стенокардии. Все пациенты относились к IV функциональному классу (ФК) по NYHA, у 3 — в анамнезе инфаркт миокарда, 3 — со стентированием коронарных артерий, 1 — с аортокоронарным шунтированием.
Отбор пациентов проводили по следующим критериям: кальцинированный АК (кальциноз 3-й степени) с преобладанием стеноза, высокий риск традиционного оперативного вмешательства при Euroscore более 20%, размер ФК АК от 22,5 до 25 мм, при гемодинамически незначимом поражении коронарных артерий и отсутствии значимой другой патологии сердца и аорты.
Для определения этих показателей пациентам выполнены следующие обследования по программе подготовки катетерной имплантации АК: трансторакальная и чреспищеводная ЭхоКГ, мультиспиральная компьютерная томография (МСКТ) с контрастированием аорты и ее ветвей, коронарография, аортография с ангиографией подвздошно-бедренного сегмента. По данным ЭхоКГ, градиент систолического давления колебался от 53 до 138 мм рт.ст. (в среднем 86±11 мм рт.ст.). Диаметр Ф.К. АК — от 22,5 до 25 мм. Площадь отверстия АК — от 0,6 до 0,9 см² (в среднем 0,72±0,2 см²). У всех пациентов был трехстворчатый АК.
Показанием для трансапикального доступа имплантации клапана служило гемодинамическое сужение подвздошно-бедренного сегмента. За 6 ч до проведения операции пациентам назначали антикоагулянтную терапию (клопидогрель 300 мг и аспирин 100 мг).
Всем пациентам установлен бескаркасный ПАК Edwards Sapien. В 7 случаях выполняли установку ПАК трансапикальным доступом, учитывая поражение подвздошно-бедренного сегмента артерий, у 5 пациентов манипуляция произведена трансфеморально. Операцию осуществляли совместными бригадами: кардиохирургами и эндоваскулярными хирургами по стандартной методике.
Интраоперационно наблюдали следующие осложнения. У 2 пациентов был спазм коронарных артерий после имплантации клапана, который потребовал введения нитратов, кардиотоников, проведения реанимационных мероприятий. После лечения при контрольной коронарографии спазм коронарных артерий ликвидирован, гемодинамика восстановлена, ЭКГ вернулась к норме. Потребовалось применение электрокардиостимуляции 1 пациенту в течение 4 дней, затем ритм восстановился. У 1 пациента была реторакотомия в связи с кровотечением в послеоперационном периоде, источник которого не установлен. Кровотечение прекратилось на фоне гемостатической терапии. Летальный исход — у 1 больного (на вскрытии обнаружено перекрытие клапаном устья левой коронарной артерии с исходом в инфаркт миокарда).
Доступ к бедренной артерии и венам выполняли для проведения ангиографии корня аорты и для выполнения стимуляции желудочков. Для проведения ангиографии аорты доступ к артерии на бедре осуществляли с использованием пигтейл-катетера размером 5—6 F, одновременно при этом вводился интродьюсер для проведения стимуляции желудочков. После установки электрода в правый желудочек проводили тест со стимуляцией желудочков с частотой от 180 до 220 уд/мин.
Выполняли левостороннюю торакотомию в V—VI межреберье, уточняя место разреза над верхушкой сердца при помощи ЭхоКГ. Перикард вскрывали, брали его на держалки. Верхушку левого желудочка (ЛЖ) выводили в рану. На мышечный сегмент верхушечно-боковой стенки ЛЖ накладывали кисетный шов на тефлоновых прокладках. После введения гепарина 5000 ЕД проводили прокол ЛЖ прямой иглой с введением в него интродьюсера размером 7 F или 8 F. Используя изогнутый катетер типа Judkins (правый), проводник размером 0,035 дюйма с J-образным кончиком проводили через клапан в нисходящую часть аорты. Проводник не должен задевать папиллярные мышцы и элементы митральных хорд, чтобы избежать осложнений в ходе введения интродьюсера и системы доставки клапана. После достижения нисходящей части аорты проводник меняли на проводник повышенной жесткости (0,035-дюймовый Amplatz Super Stiff производства компании «Boston Scientific»), а катетер типа Judkins удаляли. Интродьюсер меняли на систему доставки клапана размером 26 F, который вводили на 3—4 см в полость Л.Ж. На фоне проведения желудочковой стимуляции выполняли баллонную пластику АК с применением баллонного катетера Retroflex размером 20 мм, после этого баллон удаляли. Систему доставки Ascendra вводили в интродьюсер. Устройство клапан/катетер продвигали в аортальное положение, при этом соотношение положения клапана в аорте/желудочке оставляли в пределах 50:50. После подтверждения правильности положения клапана при помощи чреспищеводной ЭхоКГ (ЧПЭхоКГ) и ангиографии проводили желудочковую стимуляцию. Клапан устанавливали на фоне стимуляции желудочков (180 в 1 мин) и только тогда, когда АД достигало низких цифр (40—50 мм рт.ст.). После этого баллонный катетер сдували и удаляли. Проводили оценку возможной аортальной недостаточности и контроля положения клапана посредством ЧПЭхоКГ, только после этого удаляли интродьюсер из полости желудочка.
В нашем исследовании случаев аортальной недостаточности не отмечено. Однако, когда требуется провести повторное расширение клапана, то расширение клапана баллоном необходимо выполнить вновь. Область прокола ЛЖ закрывали путем затягивания кисетов на прокладках. Швы в области верхушки сердца для более уверенного гемостаза обрабатывали клеем Bioglue («CrioLife», США). Рану закрывали с оставлением дренажа в плевральной полости.
В 1 наблюдении произошло кровотечение: при повторной торакотомии источника не выявлено, при нормализации свертывающей системы крови кровотечение остановилось.
В послеоперационном периоде у всех пациентов отмечали уменьшение градиента систолического давления на клапане до 9,2±1,5 мм рт.ст. Площадь отверстия АК после операции в среднем увеличилась с 0,72±0,1 до 1,9±0,3 см².
Видео:Транскатетерная имплантация аортального клапанаСкачать

Обсуждение
Протокол обследования для пациентов, планирующихся на операцию ТИАК, должен включать следующие обследования.
ЭхоКГ — необходима для документальной фиксации степени тяжести А.С. Также необходимо исключить тяжелое поражение других клапанов сердца. Важно описать анатомию АК и наличие кальциноза, определить диаметр аортального кольца и функции ЛЖ, выявить отсутствие или наличие легочной гипертензии. Наличие выступающей перегородки на уровне выносящего тракта левого желудочка является крайне важным аспектом ввиду того, что ее наличие может помешать правильной установке клапана.
Также необходимо проведение коронарографии для выявления возможной сопутствующей ИБС. Диагностические находки требуют проведения ангиопластики до имплантации клапана. Аортография необходима для того, чтобы удостовериться в правильности положения в ходе установки клапана и для того, чтобы отметить наличие развития возможных осложнений в дуге аорты, способных помешать выполнению ТИАК. Проведение контрастной ангиографии является методом выбора оптимального операционного доступа [35]; тем не менее ее проведение не позволяет в полном и детальном объеме получить сведения об анатомических особенностях строения сосудов.
Проведение МСКТ-ангиографии является основным методом обследования больных, планирующихся на проведение ТИАК. Проведение MСКТ-ангиографии позволяет точно определить степень, длину и локализацию кальциноза сосудов, а также еще раз уточнить расстояние между устьями коронарных артерий и кольцом КА для определения возможности проведения ТИАК. При МСКТ-ангиографии возможна трехмерная реконструкция сосудов с измерением на срезе поперечного размера просвета сосудов. Минимальный диаметр просвета сосуда и длина сегмента с минимальным диаметром просвета являются основными критериями выбора доступа для осуществления доставки клапана. Применение внутрисосудистого ультразвукового исследования позволяет с помощью инвазивного способа измерить диаметр артерии; однако полученные данные могут быть неточными ввиду возможности скоса изображения.
Читайте также: Подбор шарошек для седел клапанов
Диаметр АК можно измерить с применением различных режимов визуализационных технологий: трансторакальной эхокардиографии (TTЭ), чреспищеводной эхокардиографии (ТПЭ), контрастной ангиографии, многосрезовой компьютерной томографии (МСКТ) либо МРТ-изображения. Диаметр измеряется в середине систолы на уровне прикрепления створок А.К. Ввиду отсутствия кольца для наложения швов диаметр протеза при установке посредством катетера должен быть больше (от 5 до 30%) аортального кольца для того, чтобы обеспечить стабильность положения клапана и устранения возможной парапротезной недостаточности. Само аортальное кольцо может быть не круглой формы, что может приводить к занижению размеров, полученных с помощью МСКТ. Применение МСКТ позволяет получить изображения в коронарной, сагиттальной и аксиальной проекциях АК и корня аорты, благодаря чему можно определить его максимальный и минимальный диаметры, окружность кольца и его площадь [29, 30]. Определение параметров кольца методом TTЭ либо ТПЭ применяют чаще всего. Измерение диаметра АК при помощи МСКТ с целью определения требуемых размеров клапана должно выполняться в первую очередь.
После завершения всех исследований и принятии решения о проведении ТИАК следует выбрать доступ, через который будет проводиться имплантация. Основные пути для проведения имплантации клапана Edwards Sapien (производства компании «Edwards Lifesciences») TA и Т.Ф. Оба метода доставки клапана на место имплантации одинаковы по частоте успешного проведения манипуляции и развития осложнений. Выбор будет зависеть от того, насколько извиты сосуды нижних конечностей, от наличия кальциноза артерий, от внутреннего диаметра бедренной, наружной подвздошной и общей подвздошной артерий. Наличие аневризм брюшной аорты или наличие в анамнезе операций по устранению таковой будет указывать в пользу трансапикального либо подключичного доступа. Осложнения со стороны сосудистой системы обычно сопровождаются достоверно высокими показателями летальности, поэтому их необходимо избегать с помощью проведения исследования состояния сосудов [25].
Пациенты, готовящиеся к проведению ТИАК, в большинстве своем пожилые люди, в силу чего они имеют множественные сопутствующие заболевания (ишемическая болезнь сердца (ИБС), болезни периферических сосудов, гипертония, инсульты либо транзиторные ишемические атаки). Риск операционной смертности у пациентов с сопутствующей ИБС выше, чем без нее. Перед проведением ТИАК необходимо провести реваскуляризацию сосудов, которые кровоснабжают обширную область миокарда, подверженную риску ишемии, при этом можно оставить без внимания стенозы мелких коронарных артерий [31—33]. В целом реваскуляризация перед проведением ТИАК предпочтительна в том случае, когда существует высокий риск инфаркта миокарда.
Выраженный атеросклероз дуги аорты, а также кальциноз или подвижные отложения кальция на АК считают факторами риска для развития неврологических осложнений на фоне проведения ТИАК. Всем пациентам риска следует пройти допплеровское исследование сонных артерий. При гемодинамически значимом поражении сосудов перед проведением ТИАК необходимо восстановить кровоснабжение головного мозга.
Частота успешного проведения ТИАК продолжает расти по мере того, как совершенствуется методика выполнения манипуляции и улучшаются методы отбора пациентов. Завершено первое рандомизированое исследование, в ходе которого ТИАК применяли у пациентов с высокой степенью риска при операции ПАК или у неоперабельных по любым возможным прочим причинам (AoRTiс TraNscathetER Valve — PARTNER). Это исследование позволило рекомендовать ТИАК как необходимый вид операции для лечения подобных пациентов. При этом революционным образом меняется лечение острых случаев АС и дисфункции биопротеза, когда стали возможными экстренный характер операции или проведение операции клапан-в-клапан.
Считается, что пациента следует отнести к группе высокого хирургического риска в том случае, когда показатели прогнозируемой смертности в течение 30 дней выше 15%. Риск проведения хирургического вмешательства наиболее часто оценивают по критериям Прогнозируемой Смертности (Predicted Risk of Mortality), STS-PROM, установленным Обществом Торакальных Хирургов (Society of Thoracic Surgery), и по критериям Euroscore. Критерии Euroscore проверены и на пациентах, которым выполняют операции на клапанах сердца [19, 20]. Тем не менее доказано, что данный алгоритм постоянно завышает показатели частоты случаев смертельного исхода [21, 22]. Критерии STS-PROM получены на основании показателей из базы данных Общества Торакальных Хирургов (Society of Thoracic Surgery — STS), которая является регистром, составляемым в добровольном порядке, учитывающим практические аспекты исходов операций. При использовании данных критериев проводится оценка риска летального исхода, учитываются показатели заболеваемости, наличие почечной недостаточности, продолжительность госпитализации после операции на сердце [23]. Данные критерии занижают истинные показатели частоты смертности после проведения операций на сердце, но более точно отражают прогноз смертности в хо-де проведения вмешательства и в течение следующих 30 дней в тех случаях, когда проводится ПАК с самой высокой степенью риска [24].
Критерии STS-PROM и Euroscore дают способ объективно определить степень риска. Хотя, при более тщательном рассмотрении, данные критерии риска не учитывают определенные характеристики, которые могут сильно осложнить проведение операции и повысить вероятность летального исхода, например, имевшее место ранее облучение области средостения, наличие выраженного кальциноза грудной части аорты (фарфоровая аорта), анатомические изменения стенки грудной клетки, медиастинит в анамнезе, цирроз печени либо истощенность пациента. Дряхлость больного, проявляющаяся в неспособности пациента к физической активности, является тем субъективным фактором, учет которого оказывает выраженное влияние на исход операции на сердце, но измерить данные критерии крайне сложно [3]. Применение ТИАК в обдуманном и взвешенном порядке рекомендовано для того, чтобы достигнуть максимально подходящего исхода проведения операции.
ТИАК нужно проводить в помещении для катетеризации сердечно-сосудистого отделения или в гибридной операционной, при условии, что помещение оборудовано цифровым рентгеноскопическим аппаратом с высоким качеством изображения и возможностью хранения и передачи исходных изображений для проведения операции. Должно быть достаточно места для того, чтобы работать в удобной обстановке, и есть возможность перемещать различные аппараты, такие как вакуумные отсосы, аппарат искусственного кровообращения и другие приборы вокруг операционного (рентгенологического) стола. Аппарат искусственного кровообращения должен быть рядом на случай развития осложнений. В этом же помещении должно находиться (с возможностью быстрого использования при необходимости) оборудование для проведения операций на периферических сосудах или коронарных артериях.
Операция может быть выполнена с применением общего наркоза [36, 37] или при использовании седации с сохранением сознания. Предпочтительным вариантом является наркоз с одновременным проведением ЧПЭхоКГ. В ходе всего выполнения процедуры следует проводить инвазивный мониторинг гемодинамики. Для того чтобы снизить риск инфицирования протеза, следует принимать меры асептики. В ходе выполнения операции пациенты получают антибиотики согласно утвержденным схемам.
Видео:Эндоваскулярное протезирование аортального клапанаСкачать

Заключение
ТИАК является эффективным способом лечения АС с клиническими проявлениями у крайне тяжелой категории пациентов. Дальнейшее совершенствование катетеров позволит пользоваться системами доставки клапана более малых размеров и с более легким методом установки, улучшая показатели безопасности проведения операции.
🔥 Видео
Имплантация биологического протеза клапана сердца «ТиАра»Скачать

Манчуров В.Н Транскатетерное протезирование аортального клапана.Скачать

Протезирование и Пластика клапанов сердцаСкачать

Имплантация биологического протеза клапана сердца «ЮниЛайн» АортальныйСкачать

Технология имплантации бесшовного клапана PERCEVALСкачать

Имплантация биологического протеза клапана сердца «ЮниЛайн» АтриовентрикулярныйСкачать

Протезирование аортыСкачать

Эндоваскулярное протезирование аортального клапанаСкачать

Протезирование Аортального Клапана / Aortic valve replacementСкачать

Стеноз аортального клапана: эндоваскулярное лечение трансфеморальным доступомСкачать

Протезирование аортального клапана комбинированным клапаносодержащим гомографтомСкачать