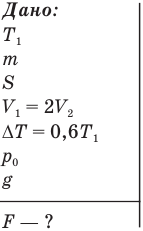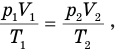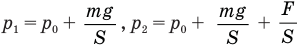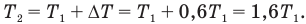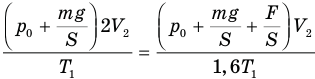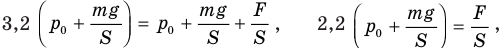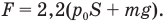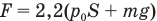- 4.3.3. Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ.
- Пример
- Решение:
- Как найти массу газа в баллоне?
- Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ
- Задача С2. В цилиндре под поршнем находится газ. Масса поршня m, площадь его основания S. С какой силой надо давить на поршень, чтобы объем воздуха под ним уменьшился вдвое и при этом температура воздуха будет повышена на 60% ? Атмосферное давление нормальное. Трением пренебречь.
4.3.3. Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ.
На данный момент задачи по этой теме кодификатора идут в КИМе ЕГЭ под номером 29.
Для их решения можно воспользоваться следующим алгоритмом:
1) записать уравнение реакции, о которой идет речь в задаче, и убедиться в правильности расставленных коэффициентов;
2) рассчитать количество молей вещества, масса или объем которого указаны в условии.
Если указана масса некого вещества A, то расчет количества вещества для него следует вести по формуле:
где mA – масса вещества А, а MA – молярная масса вещества А.
Если указан объем газообразного вещества А:
где VA – объем газообразного вещества А, а Vm – молярный объем, одинаковый для всех газов и при н.у. равный 22,4 л/моль.
Иногда вместо массы или объема вещества дается его количество вещества (моль). В таком случае действия по его нахождению не требуются.
3) далее от молей вещества А нужно перейти к молям вещества, массу или объем которого спрашивают в условии.
Допустим спрашивают объем или массу вещества B. Тогда для перехода от количества моль вещества А к количеству моль вещества B следует пользоваться тем правилом, что для любого вещества его количество, деленное на его коэффициент, в уравнении реакции одно и то же. Т.е. количества веществ А и В связаны друг с другом через коэффициенты в уравнении следующим образом:
где n(A) и n(B) – количества вещества А и В соответственно, а k(A) и k(B) – коэффициенты в уравнении перед этими веществами.
Из этого выражения следует, что количество вещества В равно:
4) далее, зная количество вещества B, мы можем найти его массу по формуле:
Читайте также: Цилиндр для замка морелли
Если же вещество B является газом и спрашивают его объем, то рассчитать его можно следующим образом:
В общем, последовательность решения таких задач можно изобразить следующей схемой:
1) Зная массу или объем вещества A, рассчитываем его количество вещества.
2) Зная количество вещества A, рассчитываем количество вещества B по формуле:
где n(A) и n(B) – количества веществ А и В соответственно, а k(A) и k(B) – коэффициенты в уравнении перед этими веществами.
3) В зависимости от того, требуется найти массу вещества В или объем газа В, умножаем его количество либо на молярную массу, либо на молярный объем газа:
Пример
Какая масса сульфида алюминия потребуется для того, чтобы в результате его взаимодействия с избытком соляной кислоты образовался газ объемом 33,6 л (н.у.).
Решение:
1) Запишем уравнение реакции:
2) Рассчитываем количество вещества, для которого известна его масса или объем (в случае газа). Нам известен объем сероводорода, рассчитаем его количество вещества:
3) Отношение количества вещества любого фигуранта реакции к его коэффициенту в уравнении этой реакции всегда одно и то же. Т.е. для сульфида алюминия и сероводорода мы можем записать, что:
Из этого выражения выразим n(Al2S3):
Подставим известные значения n(H2S) и коэффициентов перед H2S и Al2S3:
Тогда масса сульфида алюминия будет равна:
Задачи с реальных экзаменов ЕГЭ на тему «Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ» можно порешать здесь.
Как найти массу газа в баллоне?
3 сообщений
Откуда: Уфа
Кто: Специалист
Возраст: 33
Есть баллон с метаном, объемом 210 литров, с давлением 24,5 МПа! Какая масса газа уместиться в такой баллон? Желательно с формулами и пояснениями к ним
Есть баллон с метаном, объемом 210 литров, с давлением 24,5 МПа! Какая масса газа уместиться в такой баллон? Желательно с формулами и пояснениями к ним
Вот вам формула с пояснениями:
Как видите, нужно ещё знать температуру. Чем больше температура, тем меньше масса газа.
Подставляете числа в формулу и считаете.
3 сообщений
Откуда: Уфа
Кто: Специалист
Возраст: 33
Есть баллон с метаном, объемом 210 литров, с давлением 24,5 МПа! Какая масса газа уместиться в такой баллон? Желательно с формулами и пояснениями к ним
Вот вам формула с пояснениями:
Читайте также: Рассчитать объем жидкости в цилиндре вертикальном
Как видите, нужно ещё знать температуру. Чем больше температура, тем меньше масса газа.
Подставляете числа в формулу и считаете.
А в каких единицах измерения подставлять значения.
А в каких единицах измерения подставлять значения.
Главное, что бы все в одной системе. Наиболее популярная — Си.
Тогда \(P = 24.5\; МПа = 2.45 \cdot 10^7 \; Па\) ,
\(T=293\;K\) (нормальная комнатная температура).
3 сообщений
Откуда: Уфа
Кто: Специалист
Возраст: 33
А в каких единицах измерения подставлять значения.
Главное, что бы все в одной системе. Наиболее популярная — Си.
Тогда \(P = 24.5\; МПа = 2.45 \cdot 10^7 \; Па\) ,
\(T=293\;K\) (нормальная комнатная температура).
Огромное спасибо за помощь
601 сообщений
Откуда: Интернет
Кто: В поисках истины
Возраст: 34
zam, тут давление больно высокое.
У Метан Tk=190,65 К Pk=45,8 атмосферы
Плохо помню какие есть методы исследовани я веществ в критическом состоянии и как они себя видут, но думается там уже будет жидкость, а не пар.
Относительный удельный вес жидкого метана 0,555
но думается там уже будет жидкость, а не пар.
В задании сказано: «Какая масса газа. ».
Так что, условия там такие, что метан в газообразном состоянии.
601 сообщений
Откуда: Интернет
Кто: В поисках истины
Возраст: 34
но думается там уже будет жидкость, а не пар.
В задании сказано: «Какая масса газа. ».
Так что, условия там такие, что метан в газообразном состоянии.
Так Вы фразу целиком читайте. «Какая масса газа уместиться в такой баллон?»
Это не значит, что газ в болоне, это значит что закачиваем мы газ. А балон такой что сжимает газ до жидкого состояния.
Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ
а) сделать запись уравнения соответствующей условию задачи реакции. Расставить правильно стехиометрические коэффициенты;
б) сделать расчёт числа молей в-ва, количество которого указано в задаче. Если речь идёт о массе какого-то в-ва (А), то применить формулу:
Если указаны объёмы газа, то вычислять по формуле:
- VA – объём газа A;
- Vm – молярный объём, равный для всех газообразных в-в при н.у. 22,4 л/моль.
Примечание. Если кол-во вещества даётся в молях, то его находить уже не требуется.
Читайте также: Высота цилиндра площадь боковой поверхности 4 длина окружности основания 1
в) затем определить моли искомого в-ва (В), используя следствия из закона Авогадро –
- nA и nB – кол-во веществ А и В,
- kA и kB – коэффициенты перед ними в уравнении.
г) определив количество в-ва В, найти его массу:
для газообразного в-ва В использовать соответствующую формулу:
сделать расчёт кол-ва сероводорода, т.к. из условия известен его объём:
используя принцип одинаковости отношений кол-ва вещества к его стехиометрическому коэффициенту в данной реакции n(Al2S3)/k(Al2S3) = n(H2S)/k(H2S),
вычислить необходимое для реакции количество молей сульфида аллюминия:
n(Al2S3) = n(H2S)· k(Al2S3)/ k(H2S) = 1,5 моль ·1/3 = 0,5 моль
Задача С2. В цилиндре под поршнем находится газ. Масса поршня m, площадь его основания S. С какой силой надо давить на поршень, чтобы объем воздуха под ним уменьшился вдвое и при этом температура воздуха будет повышена на 60% ? Атмосферное давление нормальное. Трением пренебречь.
Задача С2. В цилиндре под поршнем находится газ. Масса поршня m, площадь его основания S. С какой силой надо давить на поршень, чтобы объем воздуха под ним уменьшился вдвое и при этом температура воздуха будет повышена на 60% ? Атмосферное давление нормальное. Трением пренебречь.
Обозначим 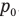
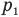
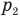
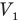
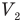
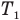
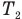
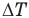
Согласно условию при неизменной массе воздуха под поршнем изменялись все три параметра его состояния: давление, объем и температура. Поэтому применим объединенный газовый закон:
С учетом условия задачи и этих равенств первое уравнение примет вид: ,
Ответ: .
Эта задача взята со страницы подробного решения задач по физике, там расположена теория и подробное решения задач по всем темам физики:
Возможно вам будут полезны эти задачи:




















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института