Область митрального клапана на эхокардиографии может быть хорошо исследована. Был использован ряд методов оценки стеноза с разной точностью.
- Планиметрический метод: он включает отслеживание внутренней границы отверстия митрального клапана в диастолу. Было показано, что эти данные хорошо коррелируют с площадью клапана, измеренной при катетеризации. Он имеет свои ограничения, особенно при наличии значительной кальцификации кончика створки, плохого определения границ и различной степени времени открытия из-за фибрилляции предсердий.
- Вена контракта: ширина струи цветного потока в двух ортогональных плоскостях коррелирует с планиметрическими расчетными значениями площади митрального клапана.
- Площадь проксимальной изоскоростной (гемисферической) поверхности (Proximal Isovelocity Area-PISA). Кровоток через суженное отверстие сходится в ряду проксимальных полушарий с изоворотами (площадь изоворотной поверхности). При митральном стенозе это может быть продемонстрировано с помощью мозаичного цветного допплера на стороне предсердий в диастолу. Скорость потока рассчитывается как 2pr2v, где r — расстояние до контура скорости v, определяемого изменением цвета на границе сглаживания. Площадь суженного отверстия может быть рассчитана путем деления пиковой скорости потока на максимальную скорость через отверстие (полученную с помощью метода непрерывного допплера). Было показано, что площадь митрального клапана, рассчитанная этим методом, коррелирует с площадью, полученной при традиционной катетеризации. Однако метод сходимости потока зависит от геометрической сложности устья митрального клапана.
- Падение давления на митральном клапане: Используя модифицированное уравнение Бернулли (4 V2), можно измерить максимальное и минимальное падение митрального давления и рассчитать среднее значение.
- Время полуспада градиента давления: это время, за которое раннее диастолическое трансмитральное давление падает до 1/2 своего пикового значения (или время, необходимое для начальной скорости, деленной на квадратный корень из 2, который равен 1,4). Затем рассчитывается митральная площадь как константа (220), деленная на давление 1/2 времени. Хотя установлено, что митральное давление 1/2 времени коррелирует с инвазивным измерением площади митрального клапана, оно также имеет серьезные ограничения, особенно у пациентов с фибрилляцией предсердий и высокой частотой сердечных сокращений. Кроме того, давление 1/2 времени зависит от сопротивления притоку левого желудочка из-за формы воронки митрального аппарата, включая компоненты как отверстия, так и состояния подклапанного аппарата. Повышенное сопротивление подклапанных структур может замедлить падение давления в приточном тракте, так что давление 1/2 времени обычно меньше, чем полученное с помощью 2D планиметрии. Противоположное явление наблюдается у пациентов с сопутствующей регургитацией на аортальном клапане или с гипертрофией левого желудочка, когда давление в 1/2 раза превышает степень митрального стеноза. Следовательно, после митральной вальвулопластики расчет может давать недостоверные значения. Основная причина недооценки точности этого метода заключается в том, что он основан на падении давления, которое часто не является экспоненциальным.
- Уравнение неразрывности: оно основано на принципе сохранения массы и энергии. Поток во всех точках вдоль трубы постоянен и равен произведению средней скорости на площадь поперечного сечения. Площадь митрального клапана рассчитывается как произведение площади поперечного сечения фиброзного кольца аорты или легочной артерии и отношения интеграла по времени соответствующей скорости клапана к скорости непрерывной волны митрального стеноза. Хотя это более сложный подход, этот метод предпочтительнее у пациентов с дополнительной значительной аортальной регургитацией, у которых давление на 1/2 времени превышает площадь митрального клапана.
В настоящее время обычной практикой является изучение большинства пациентов со значительным поражением митрального клапана с помощью чреспищеводной эхокардиографии, поскольку она обеспечивает более подробную оценку митрального клапана, подклапанного аппарата и наличия спонтанного контрастирования левого предсердия и обнаружению тромбов в ушке левого предсердия. Измерения площади митрального клапана также можно получить из чреспищеводных изображений, как описано выше. В целом площадь митрального клапана> 1,5 см2 обычно считается легким стенозом, от 1,0 до 1,5 см2 умеренным и
Эхокардиография митрального клапана (часть 4)
Оценка степени митральной регургитации на эхокардиографии
Основным фактором, определяющим тяжесть митральной регургитации на эхокардиографии, является эффективная зона регургитации, которая может быть зарегистрирована при ревматическом поражении митрального клапана, бактериальном эндокардите и митральном пролапсе. Объем регургитации 40 мл означает фракцию регургитации (объем крови, извергнутой в левое предсердие) 40% и площадь регургитации (область недостаточности митрального клапана в систоле) 40 мм2.
- Большой ударный объем ЛЖ на ЭхоКГ: увеличение конечного диастолического размера левого желудочка и падение конечного систолического размера со временем предполагает перегрузку желудочка и значительную митральную регургитацию. У этих пациентов фракционное укорочение и рассчитанная фракция выброса не должны использоваться для оценки функции желудочков. Абсолютный конечный систолический диаметр или объем можно рассматривать как более точные маркеры патологии левого желудочка на эхокардиографии. Конечный систолический диаметр> 40 мм предполагает независимый критерий недостаточности левого желудочка, обратимость которого не может быть подтверждена.
- Область цветового потока — наиболее широко используемый метод. Максимальные площади струи, отслеживаемые на разных изображениях, коррелируют с тяжестью митральной регургитации, оцененной с помощью левой вентрикулографии. Площадь регургитации> 8 см2 или относительная площадь> 40% площади левого предсердия указывает на тяжелую регургитацию, тогда как площадь струи 0,5 см2 соответствует фракции регургитации> 50%, что свидетельствует о тяжелой митральной регургитации, требующей хирургического вмешательства. Точные измерения сходимости потока кажутся более надежными, чем цветное отображение площади потока. Однако метод сходимости потока зависит от геометрической сложности отверстия регургитации, что требует поправочных факторов, как в случае эксцентрических потоков, обычно наблюдаемых при пролапсе митрального клапана.
- Вена контракта на эхокардиографии: это самая узкая область поперечного сечения струи, которая непосредственно существует у отверстия регургитации. Было обнаружено, что ширина контрактной вены коррелирует с объемом регургитации: ширина> 5 мм при объеме регургитации 60 мл предполагает тяжелую, а ширина 80 мс) конечного выброса, соответствующего снижению давления в левом желудочке во время изоволюмического периода. Короткая конечность замедления ретроградного трансмитрального сигнала предполагает значительную регургитацию. Когда давление в левом предсердии увеличивается, ретроградное падение давления на митральном клапане также падает и больше не представляет собой давление в левом желудочке. Давление в левом предсердии можно оценить как трансмитральное ретроградное падение давления, вычитаемое из систолического артериального давления, особенно когда оно низкое.
- Объем опорожнения левого предсердия: конечный систолический объем левого предсердия — конечный диастолический объем> 40 мл позволяет идентифицировать пациентов с тяжелой митральной регургитацией.
- Уравнение непрерывности на эхокардиографии: относительные ударные объемы аорты и митрального клапана с использованием уравнения непрерывности, как обсуждалось ранее, определяют тяжесть регургитации.
- Трехмерный цветной допплер: с появлением трехмерного цветного допплера в реальном времени проводятся исследования, в которых оценивается метод количественного определения объема регургитации.
Менее распространенные формы митральной регургитации на ЭхоКГ
Разрыв хорды митрального клапана. Часто это является следствием процесса миксоматозной дегенерации, который происходит с возрастом. Развитие значительной митральной регургитации обычно происходит постепенно. В некоторых случаях происходит острое начало, особенно если это не осложнение миксоматозной дегенерации, просто из-за разрыва хорд. Левый желудочек на эхокардиографии резко не расширяется. Основные симптомы — учащенное сердцебиение и одышка. Симптомы имеют тенденцию улучшаться в течение следующих недель, и к тому времени желудочек адаптируется к объемной нагрузке. В тяжелых случаях пациенты могут иметь трудноизлечимый отек легких. Это можно объяснить длительной митральной регургитацией, которая приводит к расширению и слабости левого желудочка. Сочетание повышенного желудочкового диастолического давления и давления наполнения ухудшает состояние и снижает вероятность успешного лечения.
Эндомиокардиальный фиброз. Это процесс фиброза, который затрагивает субэндокард и нижележащий слой миокарда. При поражении правого желудочка поражается преимущественно верхушка, затем прогрессирует к трикуспидальному клапану, но щадит выносящий тракт. В левом желудочке задействованы приточный отдел, верхушка и выносящий тракт. Поскольку фиброз поражает сосочковую мышцу, он приводит к регургитации митрального и трикуспидального клапанов, которая может быть достаточно серьезной, чтобы потребовать замены клапана. Это заболевание распространено в восточной части Африки, Южной Индии и Бразилии и редко поражает европейцев. Обычно это связано с гиперэозинофилией из-за глистной инфекции.
Стресс-эхокардиография. Пациентов с симптомами не более чем умеренной митральной регургитации, особенно вызванной ишемической этиологией, следует обследовать с помощью стресс-эхокардиографии. Она оценивает физиологию сердца и связанные со стрессом изменения тяжести митральной регургитации во время развития симптомов. Падение систолического артериального давления при высокой частоте сердечных сокращений также считается маркером ухудшения регургитации и быстрым снижением ударного объема крови. У пациентов с первичной болезнью левого желудочка и несоответствующей полостью может развиться повышенное давление в левом предсердии как причина их одышки при отсутствии значительной митральной регургитации. Таким образом, у таких пациентов стресс-эхокардиография может определить оптимальное лечение.
Читайте также: Клапана масляного стакана bmw m52
Лечение митральной регургитации
Легкая и умеренная митральная регургитация хорошо переносится и не требует вмешательства, кроме профилактического назначения антибиотиков по показаниям, для устранения потенциальной инфекции у пациентов с высоким риском. Тяжелая митральная регургитация, которая вызывает серьезные симптомы, несмотря на медикаментозное лечение, требует хирургического вмешательства на митральном клапане. Медикаментозная терапия включает меры по снижению давления в левом предсердии, например вазодилататоры, контроль частоты фибрилляции предсердий у пациентов с установленной аритмией, например, β-адреноблокаторы, и профилактические меры против тромбоэмболии, например варфарин.
Реконструкция митрального клапана особенно эффективна при пролапсе задней створки и иногда при пролапсе передней створки. Время операции имеет решающее значение. Хотя этот подход должен быть использован при первой возможности при разрыве сосочковой мышцы, в случае разрыва хорд его можно отложить на 1-2 недели до стабилизации гемодинамики. Это не оправдывает откладывание вмешательства до тех пор, пока у пациентов не разовьется необратимая недостаточность левого желудочка, о чем свидетельствует увеличение конечного систолического объема.
Лечение дисфункции сосочковых мышц — это лечение болезни левого желудочка с особой целью снижения диастолического давления в левом желудочке. Следует избегать замены митрального клапана при тяжелой недостаточности левого желудочка, так как она приводит к нарушению геометрии желудочков и, следовательно, функциональных характеристик. Вместо этого можно ввести митральное кольцо меньшего размера, чтобы уменьшить диаметр притока и, следовательно, регургитацию, особенно у пациентов с дилатационной кардиомиопатией, желудочек которых устойчив к медикаментозной терапии. Стресс-эхокардиография может иметь значение при выборе пациента для хирургического вмешательства. Митральная регургитация, тяжесть которой увеличивается при стрессе, по-видимому, заслуживает дальнейшего внимания по сравнению с регургитацией, которая уменьшается при стрессе и усилении укорочения базального сегмента желудочков.
Вена контракта vena contracta позволяет установить тяжесть стеноза клапана
а) Методы исследования и настройка аппарата. В настоящее время используются несколько методов эхокардиографического исследования, с помощью которых можно количественно определить степень аортальной недостаточности. Широко применявшееся до внедрения цветового допплеровского исследования допплерографическое расширенное «картирование» в импульсном режиме для определения степени аортальной недостаточности уже не играет какой-либо роли.
Хроническая аортальная недостаточность приводит к постепенному расширению левого желудочка; это подчеркивает важность определения размера левого желудочка и его сократительной функции для оценки степени аортальной недостаточности. Функция левого желудочка для оценки прогноза играет большую роль, чем степень аортальной регургитации.
С помощью цветовой допплер-ЭхоКГ, которая характеризуется высокой чувствительностью, можно быстро и надежно диагностировать аортальную недостаточность. Для этого сердце обычно исследуют из парастернальной позиции по длинной оси и из апикальной позиции двух- или пятикамерного сердца. По своей чувствительности этот метод превосходит как аускультацию, так и ангиографию. У практически здоровых лиц в 5-10% случаев выявляют небольшую, так называемую «физиологическую» регургитацию, которая занимает лишь раннюю фазу диастолы.
Для более точной оценки степени аортальной недостаточности важную роль играет оптимальная настройка ультразвукового аппарата: цветовое усиление доводят до уровня, при котором достигается максимальная интенсивность цвета струи регургитации без появления артефактов вне струи. Кроме того, рекомендуется по возможности уменьшить угол между ультразвуковым лучом и направлением струи, чтобы получить максимально возможное качество цветового изображения (8-15 МГц). Предел Найквиста сначала устанавливают в диапазоне 0,4-0,7 м/с.
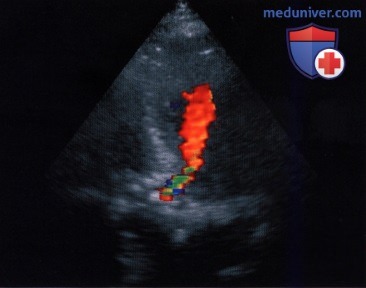
б) Площадь цветового потока. Для количественной оценки аортальной недостаточности широко распространено определение площади струи, лоцируемой методом цветового допплеровского картирования в плоскости двух или пяти камер из апикальной позиции датчика. Однако диагностические возможности данного метода исследования ограничены, поэтому корреляция между длиной, шириной и площадью профильного сечения струи и степенью тяжести аортальной недостаточности слабая. Как известно, площадь профиля струи регургитации зависит от значительно большего числа факторов, например от настройки аппарата, пред- и постнагрузки, типа струи (свободная, «пристеночная»), податливости левого желудочка и аорты. Кроме того, трудно отличить струю аортальной регургитации от входящего диастолического потока из левого предсердия, особенно при сопутствующем митральном стенозе, когда струя аортальной регургитации отклоняется в направлении митрального клапана.
Скрининг. По описанным выше причинам определение площади профильного сечения струи является лишь скрининговым исследованием, которое позволяет дать полуколичественную оценку клапанной недостаточности. Однако предсказательная ценность отрицательного результата исследования высокая, т.е. метод, как правило, позволяет исключить аортальную недостаточность, когда, несмотря на технически корректное «веерообразное» исследование всей плоскости с расположенными в ней клапанами из парастернальной и апикальной позиции датчика, струю регургитации выявить не удается. В то время как небольшая струя, расположенная вблизи аортального клапана, с высокой степенью достоверности позволяет диагностировать легкую аортальную недостаточность, при более интенсивной струе регургитации отличить умеренную аортальную недостаточность от тяжелой обычно бывает невозможно.
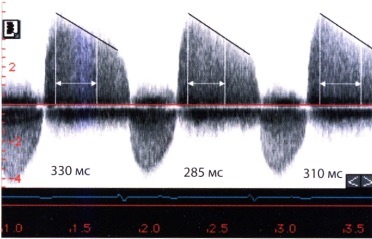
T1/2, в среднем равное 310 мс, у больного с выраженной аортальной недостаточностью.
в) Время полуспада градиента давления (РНТ или T1/2). Для определения времени полуспада градиента давления (РНТ или T1/2) проводят касательную к профилю струи. Известно, что снижение градиента давления зависит от того, как быстро происходит выравнивание давления в аорте и левом желудочке. При тяжелой аортальной недостаточности давление в аорте быстро падает, а в левом желудочке быстро нарастает. Выравнивание давления происходит очень быстро, касательная направлена круто, время полуспада градиента давления короткое. Наоборот, если выравнивание давлений происходит медленно (в случае менее выраженной аортальной недостаточности), время T1/2 становится более продолжительным.
Преимуществом метода является хорошая воспроизводимость результатов. Однако он имеет и недостаток, который состоит в том, что из-за часто отмечающейся эксцентричности струи регургитации ее направление приближается к ортогональному, и поэтому профиль кривой скорости получается недостаточно четким.
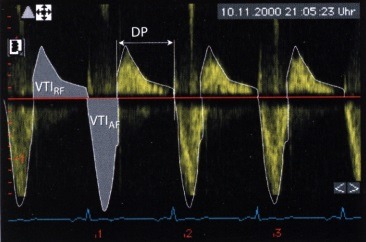
В сравнительном исследовании с помощью допплерографии и катетеризации полостей сердца время T1/2P, как маркер гемодинамически значимой аортальной недостаточности, оказалось Профиль кровотока в нисходящем отделе грудной аорты у больного с выраженной аортальной недостаточностью. Кровоток на протяжении всей диастолы ретроградный, отношение VTIRF/VTIAF=60%. VTIRF — интеграл скорости ретроградного кровотока; VTIAF — интеграл скорости антероградного кровотока.
г) Кровоток в грудной аорте. Еще одним способом количественной оценки аортальной недостаточности является ультразвуковое исследование дуги аорты и ее нисходящего отдела из супрастернальной позиции датчика. В то время как кровь через компетентный аортальный клапан во время диастолы течет в антероградном направлении, при аортальной недостаточности появляется ретроградный ток. По величине обратного диастолического кровотока в аорте можно судить о степени тяжести аортальной недостаточности. С помощью допплерографии в импульсном режиме из супрастернального доступа можно определить кровоток в нисходящей аорте, непосредственно дистальнее места отхождения левой подключичной артерии. Для количественной оценки аортальной недостаточности используют следующие параметры:
Читайте также: Двигатель z22se клапан егр
— Отношение длительности ретроградного диастолического кровотока к длительности диастолы TRF/TDiast (в процентах).
— Отношение интеграла скорости ретроградного кровотока к интегралу антероградного кровотока VTIRF/VTIAF (в процентах).
Zarauza и соавт. удалось у 45 из 51 больного (90%) получить четкий профиль кровотока в грудной аорте и с его помощью определить указанные выше параметры. В отдельных случаях профиль кровотока можно регистрировать, лоцируя брюшную аорту датчиком, располагаемым под мечевидным отростком. Контрольный объем устанавливают на расстоянии 2-3 см под диафрагмой.
Touche и соавт. и Zarauza и соавт. показали, что почти у всех больных с аортальной недостаточностью высокой степени можно обнаружить голодиастолический ретроградный ток в грудной аорте; отсутствие данного признака, как правило, позволяло исключить гемодинамически значимую аортальную недостаточность. По значению отношения VTIRF/VTIAF. разграничить умеренную аортальную недостаточность от тяжелой можно лишь условно, так как этот параметр зависит не только от степени аортальной регургитации, но и от податливости аорты и профиля скорости антероградного и ретроградного потока, который не является уплощенным ни в дуге, ни в нисходящем отделе аорты.
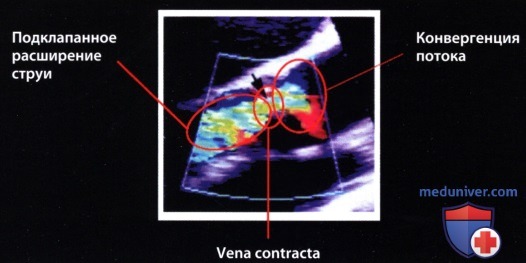
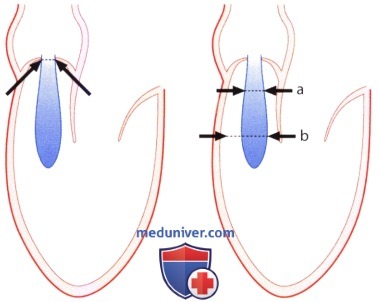

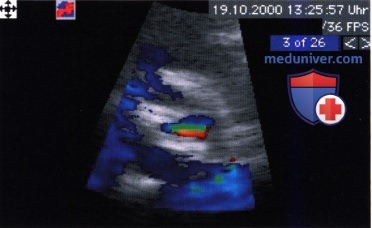
д) «Vena contracta». При аортальной недостаточности кровь из аорты забрасывается обратно в левый желудочек и достигает своей максимальной скорости в наиболее узкой части потока -на уровне так называемой эффективной площади поперечного сечения регургитации, или «vena contracta». До этого уровня поток крови ламинарный и лишь дистальнее становится турбулентным.
Эффективная площадь поперечного сечения регургитации на уровне «vena contracta» определяет объем регургитации и в принципе является наиболее информативным и наглядным параметром, характеризующим количественно аортальную недостаточность. Однако прямое измерение площади поперечного сечения на уровне «vena contracta» с помощью двумерной ЭхоКГ и цветового допплеровского картирования невозможно из-за недостаточного латерального разрешения ультразвукового луча.
В качестве «суррогата» эффективной площади регургитации можно использовать диаметр «vena contracta», измеренный с помощью двумерной ЭхоКГ. «Vena contracta» лоцируют на уровне кольца аортального клапана вдоль длинной оси сердца из парастернальной позиции датчика. Правомочность такого способа измерения для количественной характеристики аортальной недостаточности доказана в ряде исследований. Этот способ имеет существенные преимущества перед измерением ширины струи регургитации, так как на уровне «vena contracta» ток ламинарный и условия измерения воспроизводимы. Дистальнее «vena contracta» ток становится турбулентным, поэтому на ширину струи влияет множество факторов, которые существенно снижают воспроизводимость результатов определения этого параметра. Струя регургитации из-за появляющейся турбуленции уже в проксимальном своем отделе шире, чем «vena contracta». Ширина струи регургитации, в отличие от ширины «vena contracta», зависит от настройки аппарата, гемодинамических условий и податливости принимающей камеры.
В исследовании Tribouilloy и соавт. у 79 больных с аортальной недостаточностью ширина струи регургитации составила 10±5 мм и тем самым оказалась вдвое шире, чем диаметр «vena contracta», который был равен 5±2 мм. Принципиальное различие между этими двумя параметрами представлено на рисунке ниже. Отношение ширины струи регургитации к диаметру выносящего отдела левого желудочка (граничное значение для аортальной недостаточности составляет более 40%) более предпочтительно для количественной характеристики аортальной недостаточности, чем изолированное измерение диаметра «сжатой вены». В упомянутом выше исследовании Tribouilloy и соавт. выявлена корреляция между диаметром «vena contracta» и определенной эхокардиографически площадью сжатого сечения струи регургитации. Корреляция отмечена как в отношении эксцентрической, так и концентрической струи. Гемодинамически значимую аортальную недостаточность (с выбранной для нее в качестве критерия площадью поперечного сечения струи регургитации >30 мм 2 ) при граничном значении диаметра «vena contracta» >6 мм можно было бы предсказать с чувствительностью 95% и специфичностью 90%. На рисунке ниже показана «vena contracta» у больных с легкой и тяжелой аортальной недостаточностью.
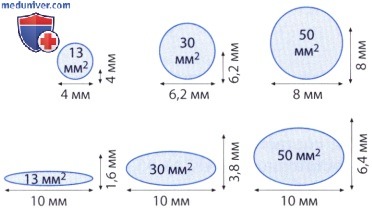
1. Ограничения данного параметра. Примерно в 30% случаев, особенно когда струя регургитации бывает множественной или эксцентричной, при двустворчатом аортальном клапане, при кальцинозе клапана и при расширении аорты может оказаться невозможно или во всяком случае трудно точно измерить диаметр «vena contracta». В таких случаях ищут альтернативные позиции для установления датчика; его, например, можно установить в парастернальную позицию справа или слева на уровне второго или третьего межреберья в положении больного на правом боку или лоцировать «vena contracta» при ЧПЭ. Наконец, следует отметить, что сжатое сечение струи регургитации лишь в очень редких случаях имеет округлую форму, и только в этих случаях можно на основании диаметра «vena contracta», измеренного с помощью двумерной ЭхоКГ, математически корректно рассчитать площадь сжатого сечения струи регургитации. При округлом сжатом сечении струи регургитации площадью 30 мм 2 диаметр «vena contracta» составляет 6,2 мм независимо от направления ультразвукового луча. При щелевидном сжатом сечении струи регургитации для такого же значения площади «сжатая вена», как показано на рисунке 17.29, в одном измерении может быть равна 3,8 мм, в другом — 10 мм. Эту особенность при измерении диаметра «vena contracta» с помощью двумерной ЭхоКГ не учитывают, что может стать причиной как заниженной, так и завышенной оценки аортальной недостаточности.
2. Новые подходы. Принципиально новый многообещающий подход для решения этой проблемы дает трехмерная реконструкция струи регургитации в области «vena contracta». Альтернативным методом является определение объема регургитируемой крови как интеграла допплеровской «мощности» (количество отражающих частиц) и умноженной на линейную скорость кровотока на уровне «vena contracta». Уже в ранее проведенных исследованиях была показана возможность определения степени регургитации по интенсивности сигнала, получаемого при непрерывноволновой допплерографии. Однако в этих исследованиях соотношение между интенсивностью сигнала и объемной скоростью существенно варьировало, так как интенсивность допплеровского сигнала отражала турбулентность всей струи регургитации в целом. Однако Buck и соавт., пользуясь в эксперименте и клинике методикой, при которой исследуют лишь ламинарный ток на уровне «сжатой вены», получили многообещающие результаты, свидетельствующие о возможности количественной оценки аортальной недостаточности.
е) Прямое определение площади поперечного сечения струи регургитации. Для того чтобы учесть неправильную конфигурацию поперечного сечения струи регургитации, появляется все больше сторонников прямой визуализации этого сечения на уровне «vena contracta» и планиметрического определения его площади. Однако следует учесть, что ламинарный поток крови на уровне «vena contracta» лоцировать в направлении, перпендикулярном направлению движения струи, невозможно. Если при цветовом допплеровском картировании удается визуализировать струю регургитации, следует, лоцируя сердце вдоль короткой оси, получить косой срез на уровне «vena contracta» или турбулентной части струи.
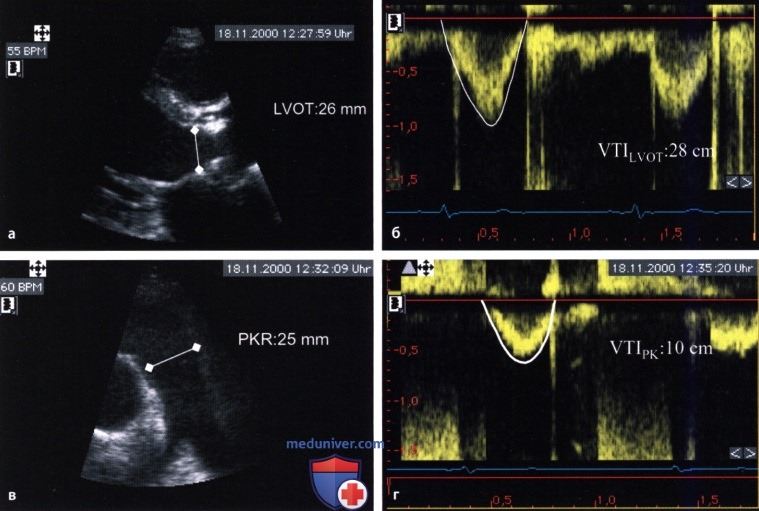
Определение фракции регургитации (ФР) у больного с тяжелой аортальной недостаточностью (IV степень):
а — Определение диаметра выносящего тракта левого желудочка (LVOT) при двухмерной ЭхоКГ.
б — Определение интеграла линейной скорости систолического трансаортального кровотока (VTILVOT).
в — Определение диаметра пульмонального клапанного кольца (PKR).
г — Определение интеграла линейной скорости систолического транспульмонального кровотока (VTIRK).
Расчет фракции аортальной регургитации (ФР):
1. Ударный объем (SVLVOT) на уровне выносящего тракта левого желудочка: SVLVOT = 1,3 2 • π • 28 = 149 мл.
2. Ударный объем на уровне пульмонального клапанного кольца: SVRK = 1,25 2 • π • 10 = 49 мл.
3. Объем регургитации: SVрег= SVLVOT— SVРК = 149-49 = 100 мл.
4. Фракция регургитации: RF = SVрег/SVLVOT= 100/149 = 0,67 = 67%.
Читайте также: Электрическая схема дэу нексия 16 клапанов 2007
ж) Количественное допплеровское исследование. Эффективную площадь поперечного сечения струи регургитации аналогично площади отверстия аортального клапана при его стенозе (см. выше) рассчитывают на основании уравнения непрерывности потока.
1. Объем регургитации (SVрег). Объем регургитации вычисляют как разницу между общим объемом крови, протекающей через аортальный клапан во время систолы SVtotal и эффективным ударным объемом SVeff:
2. Общий объем крови SVtotal. Для измерения общего объема крови SVtotal существуют два метода:
— Определение ударного объема в выносящем тракте левого желудочка.
— Волюметрическое определение ударного объема левого желудочка по модифицированному методу Симпсона.
3. Эффективный ударный объем SVeff. Эффективный ударный объем крови SVeff определяют:
— либо на клапане легочной артерии,
— либо на митральном клапане.
Ударный объем, определенный на клапане легочной артерии и на митральном клапане, соответствует произведению площади отверстия соответствующих клапанов на интеграл линейной скорости, измеренной с помощью допплерографии. На точность определения ударного объема особенно сильно влияет измерение диаметра клапанного кольца, так как в формуле для определения ударного объема значение диаметра возводят в квадрат. При измерении диаметра клапанного кольца легочной артерии, которое осуществляют обычно, лоцируя его вдоль короткой оси из парастернальной позиции, латеральный край кольца виден нечетко. Определение ударного объема на митральном клапане также сопряжено с трудностями при измерении митрального кольца. Митральное кольцо имеет эллиптическую форму, поэтому площадь отверстия митрального клапана рассчитывают, используя значение двух осей эллипса, измеренных в плоскости четырех камер (d4K) и в плоскости двух желудочков (d2K): площадь отверстия митрального клапана SMK = d4K * d2K * π/4.
Этот метод трудоемкий, и, кроме того, при измерении размеров клапана ультразвуковой датчик далеко отстоит от клапанного кольца, а латеральное разрешение ультразвукового луча недостаточное. Наконец, использовать данный метод в тех случаях, когда имеется митральная недостаточность, невозможно. Учитывая перечисленные выше недостатки метода измерения размеров митрального клапанного кольца, мы предпочитаем определять ударный объем на клапане легочной артерии.
4. Фракция регургитации RFAO. Фракцию регургитации определяют как отношение объема регургитации к общему объему выбрасываемой крови:
При фракции регургитации менее 30% говорят о легкой аортальной недостаточности (AI 1+). Фракция регургитации, равная 30-45%, соответствует умеренной аортальной недостаточности (AI 2+), 45-60% — тяжелой (AI 3+), более 60% — очень тяжелой (AI 4+).
5. Эффективная площадь поперечного сечения струи регургитации (ЭПР). Эффективную площадь поперечного сечения струи регургитации, как было упомянуто выше, рассчитывают в соответствии с уравнением непрерывности потока на основании объема регургитации SVрег и интеграла линейной скорости струи регургитации (VTIрег), измеренных с помощью непрерывноволновой допплерографии:
Этот параметр, по сравнению с объемом регургитации и фракцией регургитации, в меньшей степени зависит от пред- и постнагрузки левого желудочка.
6. Граничные значения. Для гемодинамически значимой аортальной недостаточности выведены следующие граничные значения: площадь поперечного сечения струи регургитации более 30 мм 2 , объем регургитации более 60 мл и фракция регургитации более 45%.
7. Значение количественного допплеровского исследования. Описанные методики расчета гемодинамических параметров с помощью допплеровского исследования очень трудоемкие и требуют от исследователя большого опыта. Многочисленные измерения, которые приходится выполнять, становятся причиной ошибок и снижают воспроизводимость результатов. Как и в случае других сложных параметров, параметры, которые были здесь рассчитаны, лишь тогда могут найти широкое применение в клинической практике, когда более простые показатели, на которых они основываются, удастся точно определить.
д) Конвергенция проксимальной части потока. Концепция «конвергенции проксимальной части потока» (Proximal Isovelocity Surface Area — PISA), разработанная для количественной оценки клапанной недостаточности, основывается на феномене, суть которого сводится к тому, что кровь, протекая через отверстие несостоятельного клапана, ускоряется в так называемой зоне конвергенции. В этой зоне все клетки крови, движущиеся с одинаковой скоростью, распределяются по условной полусферической поверхности, центр которой находится в регургитационном отверстии. Зона конвергенции формируется из многочисленных концентрических полусфер, окружающих регургитационное отверстие. В принципе, согласно уравнению непрерывности потока, объемная скорость потока, рассчитываемая как произведение площади поверхности полусферического слоя на линейную скорость кровотока, для разных слоев одинакова. Чем меньше радиус полусферы, тем выше линейная скорость на ее поверхности. С помощью цветового допплеровского картирования можно «окрасить» полусферические слои соответственно предельной скорости Найквиста в разные цвета на допплеровском изображении.
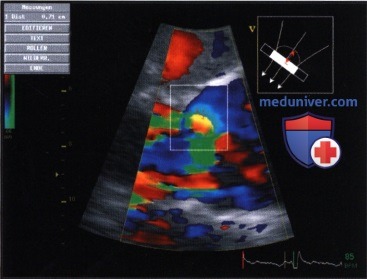
На рисунке ниже показана зона конвергенции, зарегистрированная у больного с гемодинамически значимой аортальной недостаточностью. Зная заданный предел Найквиста V (в нашем случае он равен 69 см/с) и радиус r полусферы в середине диастолы (равен расстоянию от зон, окрашенных в разный цвет, до регургитационного отверстия — в данном случае 0,71 см), можно рассчитать объем регургитации Q:
Q (мл/с) = 2π х r 2 • V = 2л • 0,71 2 см/с = 218 мл/с.
Зная объем регургитации Q и определив путем перемещения датчика в апикальную позицию среднюю линейную скорость струи регургитации, можно рассчитать эффективную площадь поперечного сечения струи регургитации (А):
А = Объем регургитации/Средняя линейная скорость струи регургитации в диастолу = 218/300 = 0,72 см 2 .
Недостатки метода. Следует отметить следующие недостатки концепции конвергенции проксимальной части струи:
— Участки струи с одинаковой линейной скоростью часто образуют не полусферы, а чашеобразные оболочки, имеющие разную ширину и высоту.
— Регургитационное отверстие при аортальной недостаточности часто имеет не округлую форму, которая необходима для расчетов в соответствии с концепцией конвергенции проксимальной части потока, а приобретает весьма сложную конфигурацию из-за изменений, обусловленных эндокардитом или пролапсом створок аортального клапана.
— Обызвествление аортального клапана и стенки аорты влияют на геометрию зоны конвергенции.
— Аорта препятствует латеральному отклонению зоны конвергенции, что может привести к завышенным значениям объема регургитации.
В целом, валидность метода, основанного на концепции конвергенции проксимальной части потока при количественной оценке аортальной недостаточности, пока окончательно не доказана, и поэтому он не получил широкого применения. Его можно использовать наряду с другими методами при определении степени тяжести аортальной недостаточности: минимальная или слабая конвергенция струи регургитации через аортальный клапан говорит о легкой аортальной недостаточности, в то время как выраженная конвергенция соответствует тяжелой аортальной недостаточности. При ортогональном расположении зоны конвергенции относительно направления лоцирования можно воспользоваться приведенными в работе Giesler и соавт. критериями тяжелой аортальной недостаточности (PISA-радиус >0,7 см при пределе Найквиста не менее 30 см/с).
е) Заключение. Описанные методы из-за перечисленных недостатков по своей диагностической ценности ограничены, поэтому часто бывает целесообразно для повышения достоверности диагноза применять их вместе. Если при использовании двух методов получают примерно одинаковую количественную оценку степени тяжести, то ее можно считать достоверной. Так, о легкой аортальной недостаточности можно говорить в том случае, когда при лоцировании в плоскости четырех камер из апикальной позиции датчика выявляют цветную струю лишь в непосредственной близости от клапана и одновременно преимущественно антероградный кровоток в грудной аорте во время диастолы.
О тяжелой аортальной недостаточности говорят в том случае, если ширина струи регургитации на уровне «vena contracta» равна 7 мм и более, а РНТ (Т1/2P)